
1
Forth stage
Medicine
Lec-2
د.ضياء الليلة
1/1/2014
Celiac disease
An immunologically mediated inflammatory disorder of the small bowel
Occurring in genetically susceptible individuals Resulting from intolerance to wheat gluten
and similar proteins found in rye, barley and, to a
lesser extent, oats.
Prevalence
The condition occurs world-wide but is more common in northern Europe.
The prevalence in the UK is approximately 1%, although 50% of these people are
asymptomatic
Pathogenesis
1. Enviromental factors:
Gluten (grain proteins)the “disease-activating protein,” is found in wheat, rye, and
barley.
2. Genetic factors:
a. Frequent intrafamilial occurrence of celiac disease
Concordance for CD in first-degree relatives ranges between 8% and 18% and
reaches 70% in monozygotic twins
b.. More than 95% of celiac patients have the isoform of DQ2 or DQ8
Pathophysiology
The precise mechanism of mucosal damage is unclear but immunological responses to
gluten play a key role .
1. Gluten will be taken up by epithelial cells.
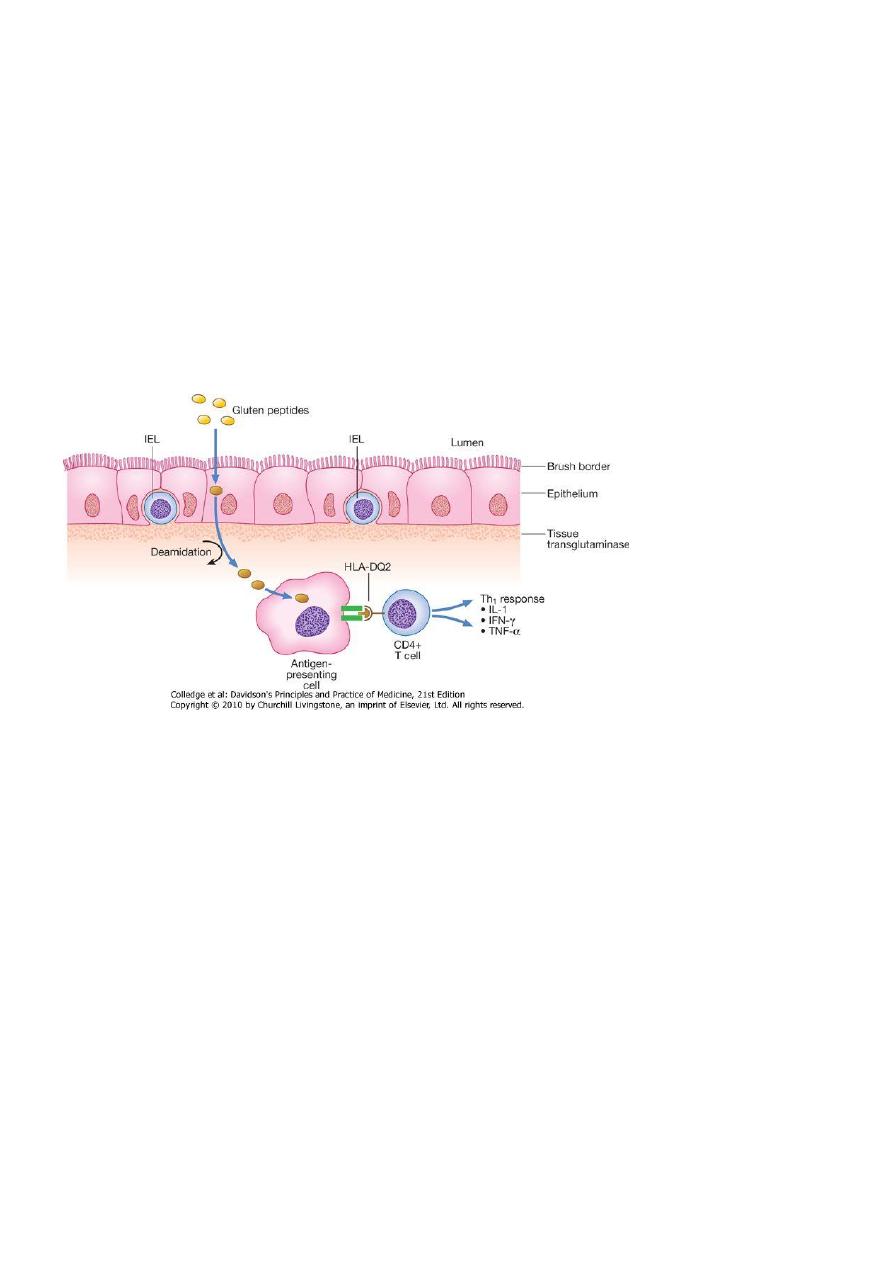
2
2. Gluten peptides will be deaminated by by the enzyme tissue transglutaminase in the
subepithelial layer.
2. They are then able to fit the antigen-binding motif antigen-presenting cells in the lamina
propria that express HLA-DQ2 or HLA-DQ8
immune response with
1
3. Recognition of gliadin peptides by CD4+ T cells triggers a Th
generation of pro-inflammatory cytokines (IL-1, IFN-γ and TNF-α).
These lymphocytes then activate B lymphocytes to generate immunoglobulins
4. Lymphocytes infiltrate the lamina propria, and increased intraepithelial lymphocytes
(IEL), crypt hyperplasia and villous atrophy ensue
Adult celiac
1. Peak age of onset: the third or fourth decade
2. Sex: females are affected twice as often as male
3. The presentation is highly variable, depending on the severity and extent of small bowel
involvement.
Classifications
1. Classical: Patients who present with GI symptoms (<50%)
2. Atypical: Present with extra intestinal manifestations only (>50%).
3. Silent: Gluten-induced inflammation without symptoms or signs.

3
1.Classical (GI manifestations)
A. Usually subtle and non-specific symptoms (for example, non-specific abdominal pain,
symptoms similar to those of irritable bowel syndrome, or even upper gastrointestinal
symptoms (dyspeptic symptoms) and weight loss.
B. Much less commonly present with symptoms of malabsorbtion including diarrhea,
flatulence, abdominal distention, weight loss, malaise, steatorrhea.
2. Atypical
Extra intestinal features that include:
• Anaemia (iron deficiency or dimorphic anemia)
• Short stature and delayed puberty
• Recurrent fetal loss and infertility
• Bone fractures and osteoporosis
• Psychiatric syndromes (depression)
Other manifestations
• Neurological disorders: such as ataxia, peripheral neuropathy, and seizures
• Dental enamel defects
• Fatigue or "tired all the time"
• Arthralgia, arthritis, and myalgia
• Skin rash (dermatitis herpetiformis) and aphthous ulcers, alopecia areata.
Diseases associations of coeliac disease
Systemic diseases:
Type 1 diabetes mellitus (2-8%)
Thyroid disease (5%)
Primary biliary cirrhosis (3%)
Sjögren's syndrome (3%)
IgA deficiency (2%)
Pernicious anemia
4
Diagnosis
1. Serology(while the patient is on gluten-rich diet)
2. Upper endoscopy and duodenal biopsy
3. Genetic studies (HLA test) rarely requested
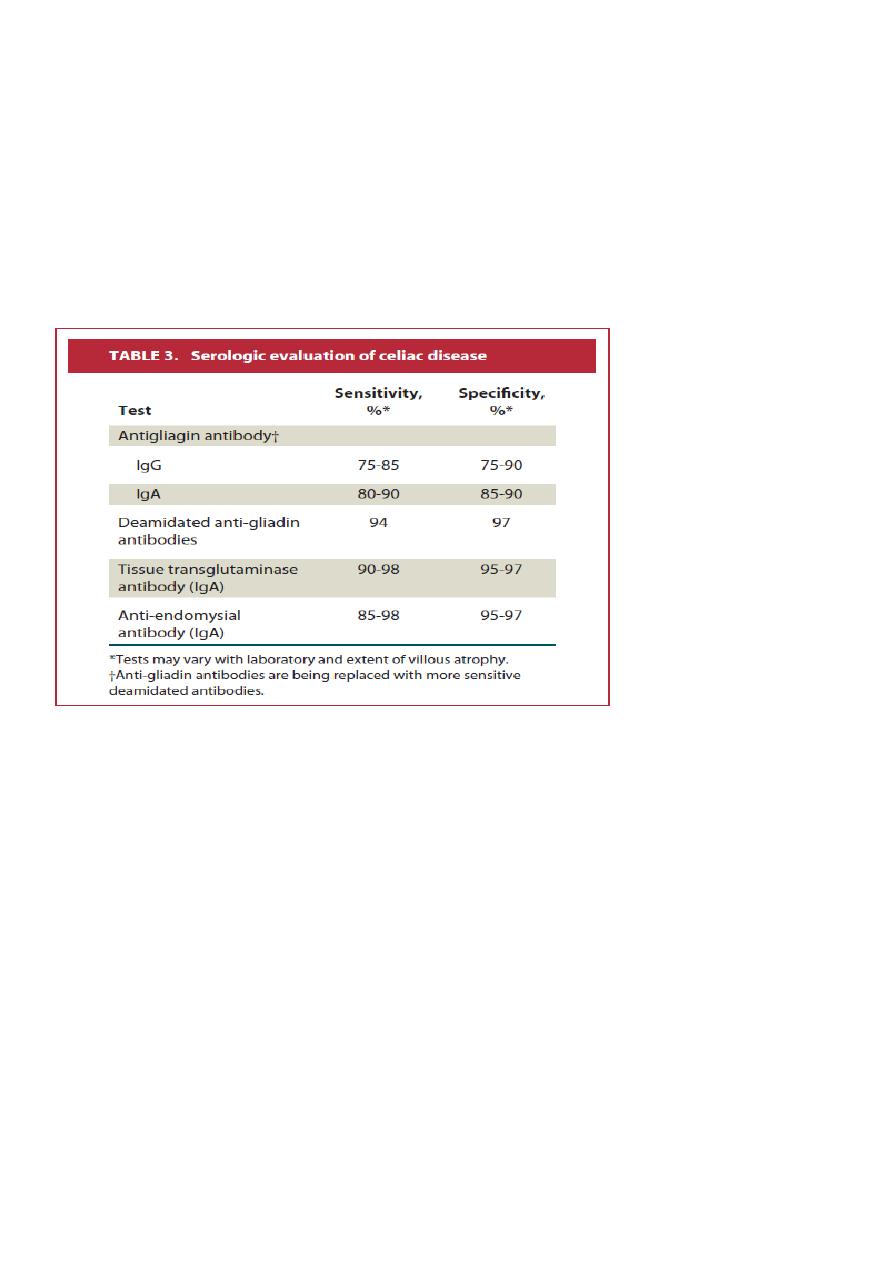
1. Serological Tests
a - IgA antitTG (tissue transglutaminase) antibodies (detected by ELISA).
This test is used for first-level screening of CD because it is an accurate, easy to perform,
and operator-independent test.
b- Serum IgA class antiendomysial antibodies
(detected by indirect immunofluorescence).
It has a higher positive predictive value
2. ENDOSCOPY
Indications:
1. Patients with clinical features of celiac disease
2. Patients with positive serology (positive EMA or tTG antibodies)
5
A low threshold for endoscopic referral is appropriate, even if serologic study results are
negative because approximately 10% of patients with celiac disease have negative serologic
results.
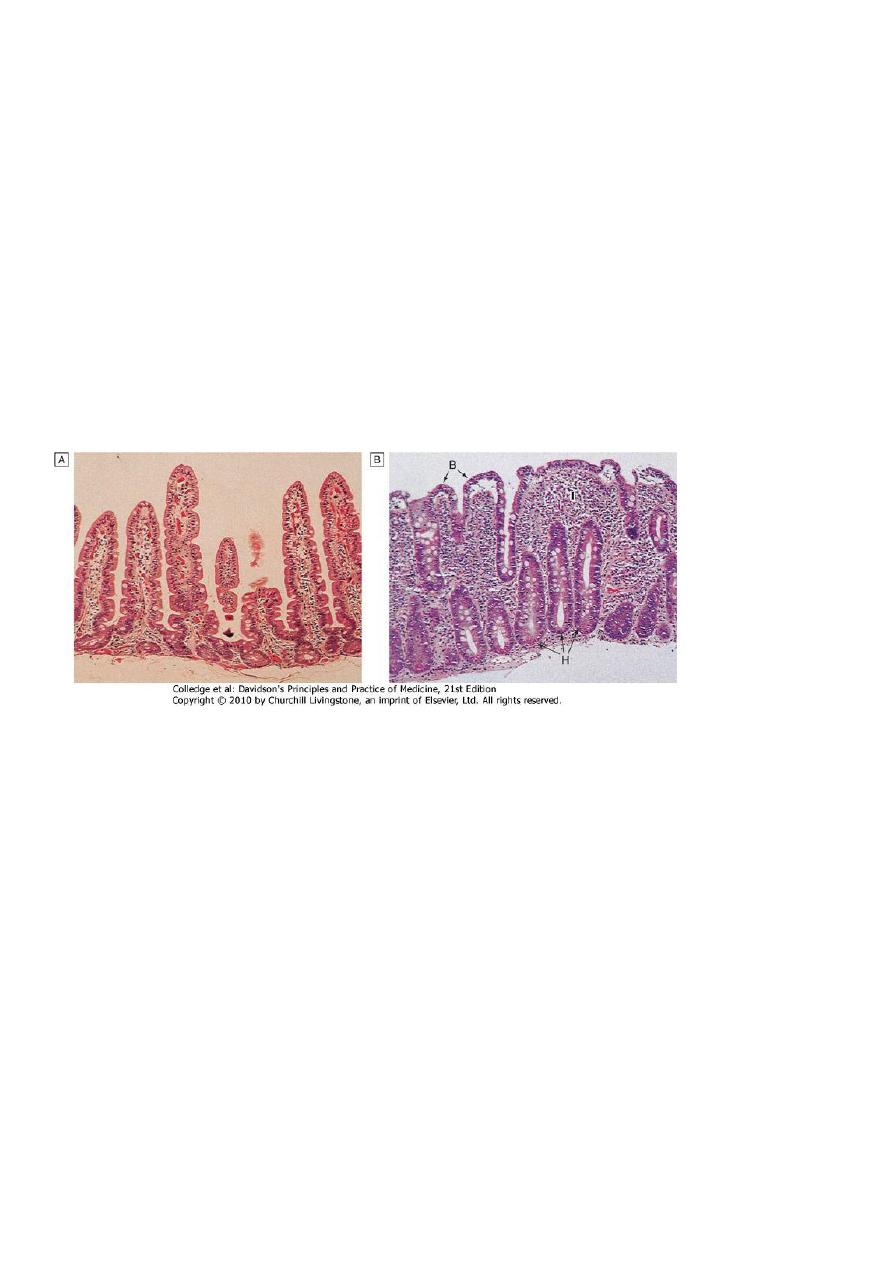
Small Bowel biopsy
Endoscopic small bowel biopsy is the gold standard.
The histological features:
1.Partial, subtotal or total villous atrophy.
2. Sometimes the villi appear normal but there are excess numbers of intra-epithelial
lymphocytes present
Causes of villous atrophy
Coeliac disease
Tropical sprue
Viral gastroenteritis
Dermatitis herpetiformis
Lymphoma
AIDS enteropathy
Giardiasis
Hypogammaglobulinaemia
Radiation
Whipple's disease
Zollinger-Ellison syndrome
The biopsy is not 100% sensitive or specific Hence, a clinical response to gluten withdrawal
is a crucial step in establishing the diagnosis

6
Hematology and Biochemistry
1. Microcytic or macrocytic anaemia from iron or folate deficiency
2. Hypocalcemia
3. Hypoalbuminemia
4. Hypomagnesemia
5. Low vitamin D level
Management
The aims are :
1. To correct existing deficiencies of iron, folate, calcium and/or vitamin D.
2. To commence a life-long gluten-free diet.
This requires the exclusion of wheat, rye, barley and initially oats, although oats may be
reintroduced safely in most patients after 6-12 months..
Mineral and vitamin supplements are also given when indicated but are seldom necessary
when a strict gluten-free diet is adhered to.
Regular monitoring of symptoms, weight and nutrition is essential.
Complications of celiac disease
a. Ulcerative jejuno-ileitis
b. Enteropathy-associated T-cell lymphoma
1.Ulcerative jejuno-ileitis
Few patients develop ulcerative jejuno-ileitis;
Fever, pain, obstruction or perforation .
Treatment: corticosteroids or immunosuppressive drugs to induce remission
2. Small bowel lymphoma
The greatest risk is for small-bowel lymphoma.

7
Also whether compliance with diet influences the rates of these cancers is debatable:
Vigilance for the increased cancer risk is warranted
1. Change of pattern of GI symptoms.
2. Recurrence of malabsorption.
3. Occurrence of alarm symptoms (weight loss, severe abdominal pain)
Risk of mortality and malignancy
There is an increase in mortality in patients with celiac disease
Increased rates of malignancy including:
Enteropathy-associated T-cell lymphoma
Small bowel carcinoma
Squamous carcinoma of the oesophagus
Head and neck cancers
non-Hodgkin’s lymphoma
Colorectal cancer
Hepatocellular carcinoma
Chronic pancreatitis
Definition: A chronic inflammatory disease characterized by fibrosis and loss of exocrine
and endocrine pancreatic function in advanced cases.
Clinical manifestations
Abdominal pain
The pain is typically epigastric, often radiates to the back, is occasionally associated with
nausea and vomiting, and may be partially relieved by sitting upright or leaning forward.
The pain is often worse 15 to 30 minutes after eating.

8
Early in the course of chronic pancreatitis, the pain may occur in discrete attacks; as the
condition progresses, the pain tends to become more continuous
Aetiology
- Alcohol abuse: the commonest cause.
- Cigarette smoking : associated with both acute and chronic pancreatitis
- Genetic causes ( hereditary pancreatitis)
- Tropical pancreatitis
- Systemic disease such as systemic lupus erythematosus, hypertriglyceridemia, possibly
hyperparathyroidism
- Autoimmune pancreatitis
- Idiopathic pancreatitis
- Exocrine pancreatic insufficiency :
- clinically significant protein and fat deficiencies do not occur until over 90 percent of
pancreatic function is lost.
- Fat malabsorption occur first
- Malabsorption of the fat soluble vitamins (A, D, E, K)
- Endocrine pancreatic insufficiency
- Pancreatic diabetes:
- - Glucose intolerance occurs with some frequency in chronic pancreatitis.
- - Overt diabetes mellitus usually occurs late in the course of disease
Diagnosis
Can be difficult since laboratory studies and imaging procedures may be normal.
Investigations:
1. Imaging studies: Abdo.x-ray, USG, CT, MRI, MRCP, Endo.USG
2. Tests of pancreatic functions.
Plain films
Calcifications within the pancreatic duct are present on plain film in approximately 30
percent of patients with chronic pancreatitis-
USG, CT, MRI
Transabdominal ultrasonography (US), CT scan, and MRI may show:
- Calcifications.
- Ductal dilatation.

9
- nlargement of the pancreas (atrophy in later stages).
- Fluid collections (eg, pseudocysts) adjacent to the gland.
Magnetic resonance cholangiopancreatography (MRCP)
MRCP is becoming the diagnostic test of choice since it can demonstrate calcifications
and pancreatic duct abnormalities consistent with chronic pancreatitis.
Endoscopic ultrasonography
The presence of four or more of these features to be highly suggestive of chronic
pancreatitis
Dilation of the main pancreatic duct.
An irregular main pancreatic duct
Hyperechoic margins of the main pancreatic duct.
Visible side branches.
Cysts
Lobularity.
Hyperechoic foci and strands
Pancreatic function test
_direct
_indirect
Direct
1.
Involve the stimulation of the pancreas through the administration of a meal or
hormonal secretagogues.
After which duodenal fluid is collected and analyzed to quantify normal pancreatic
secretory content (ie, enzymes, and bicarbonate).
2. Indirect
They measure the consequences of pancreatic insufficiency
However, they depend upon the consequences of pancreatic maldigestion, which are
generally not apparent until normal enzyme secretory output has declined by more than
90 percent.
Thus, they are insensitive to early pancreatic insufficiency.

11
Pancreatic Exocrine dysfunction
1. Fecal fat estimation:
-
Qualitative: by Sudan staining of feces
Quantitative: A 72-hour quantitative fecal
fat
-
2. Fecal elastase measurement:
Management
1. Avoidance of alcohol
2. Pain relief:
a. Simple analgesia.
b. Opiate : for relief of severe pain (problem of addiction).
c. Oral pancreatic enzymes supplements act by suppressing pancreatic secretion.
d. Endoscopic therapy :aimed at decompressing an obstructed pancreatic duct can be
associated with pain relief in some patients
e. Surgery: for patients who fail medical therapy. Four surgical approaches have been
described: Decompression
Drainage operations
Pancreatic resections
Denervation procedures.
Some surgical procedures employ a combination of these approaches
Malabsorption
1. Dietary fat restriction with supplementary medium-chain triglyceride in
malnourished patients.
2. Oral pancreatic enzyme supplement with PPI to optimize duodenal pH for
pancreatic enzyme activity.
