
1
Cancer Chemotherapy
linrong
Department of pharmacology

2
Cancer chemotherapy
n
Growth fraction
n
Proliferating cells , Non-proliferating cells
n
Mechanisms of Antineoplastic Drugs
n
Toxicity of Antineoplastic Drugs
n
Classification of Antineoplastic Drugs
n
Principles of combination therapies
phase of proliferation cycle
source and action mechanisms

3
General Introduction
n
Cancers account for 20-25% of deaths in
clinical practices.
n
Attempts to cure or palliate cancer employ 3
principal methods:
operation
,
radiotherapy
,
and
chemotherapy
.
n
Differing from the operation and radiotherapy
that emphasize on the treatment of local
tissues,
the chemotherapy is concerned with
that of the whole body.

4
Cancer chemotherapy
n
Chemotherapy is the use of drugs to
inhibit or kill
proliferating cancer cells,
while leaving host cells unharmed, or at
least recoverable.

5
Growth fraction
n
Tumor cells can be classified as
proliferating
cells
and
non-proliferating cells
.
n
The ratio of proliferating cells in the whole
tumor tissue is called
growth fraction
(
GF
).
n
The faster the tumor cells proliferate, the
bigger the GF is and the higher the sensitivity
of tumor to a drug is.
n
Generally,
in the early stage, the GF of a
tumor is bigger and the effect of a drug on
the tumor is better
.

6
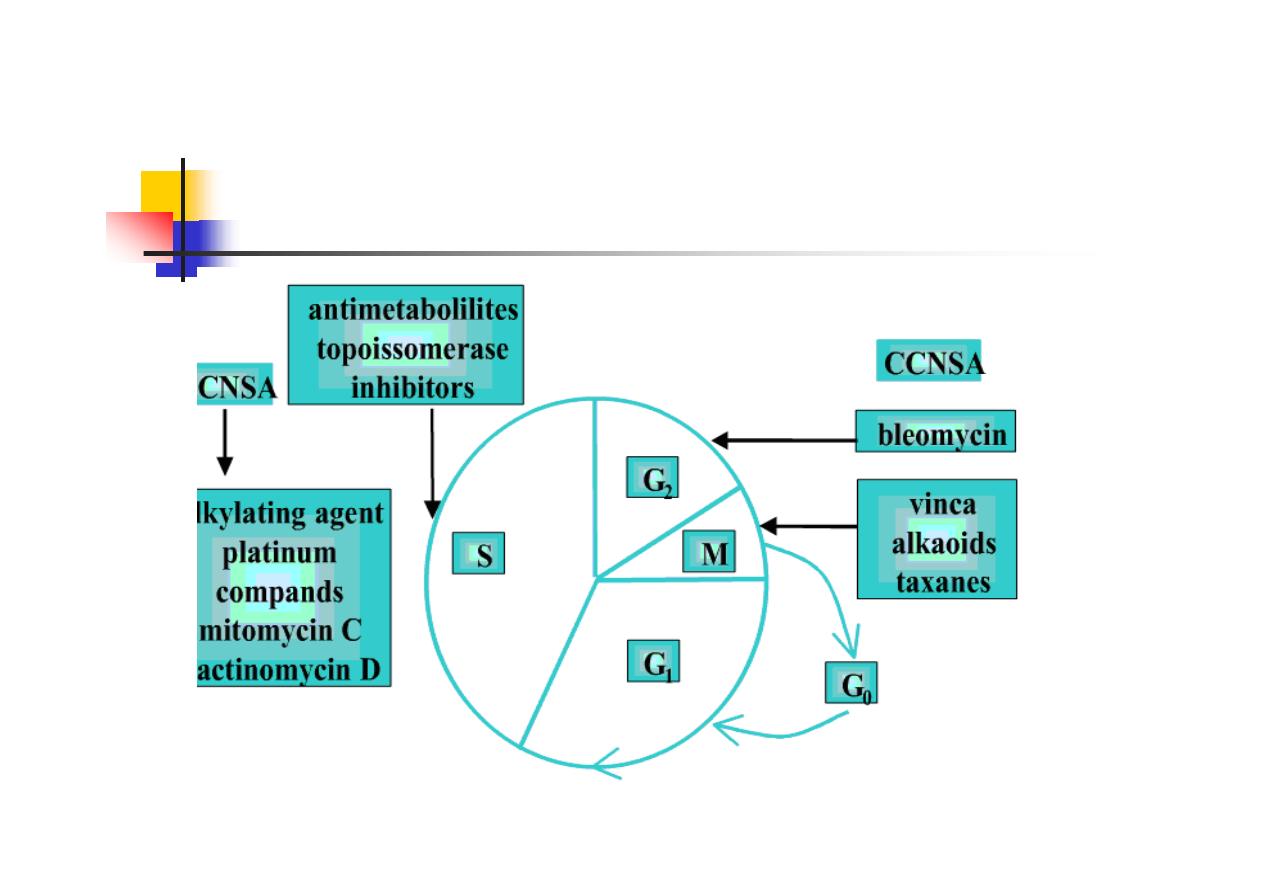
q
Proliferating cells
Based on the
DNA changes
in cells, proliferating cycle of tumor
cells can be divided into 4 phases
v
Pre-synthetic phase
(Gap 1 phase or
G1 phase
). cells chiefly
make preparations for the synthesis of DNA.
v
Synthetic phase
(
S phase
). cells are synthesizing their DNA.
v
Post-synthetic phase
(Gap 2 phase or
G2 phase
). DNA
duplication has been finished and they are equally divided to
the two of future sub-cells.
v
Mitosis phase
(
M Phase
). each cell is divided into two sub-
cells. Some of these new cells enter the new proliferating
cycle, the others become non-proliferating cells.
7
q
Proliferating cells

8
Non-proliferating cells
n
Non-proliferating cells include
G
0
phase cells
(
resting-phase cells
),
n
G
0
phase cells have proliferation ability but do not
divide temporally.
n
When proliferating cells are suffered
heavy casualties,
G
0
phase cells will get into proliferating cycle and
become the reasons of tumor recurrence.
n
G
0
phase cells are usually
not sensitive to
antineoplastic drugs
, which is the important obstacle
to tumor chemotherapy.

9
Cancer chemotherapy
n
Growth fraction
n
Proliferating cells , Non-proliferating cells
n
Mechanisms of Antineoplastic Drugs
n
Toxicity of Antineoplastic Drugs
n
Classification of Antineoplastic Drugs
n
Principles of combination therapies
Ødestruction of DNA or inhibition of DNA duplication
Øinhibition of nucleic acid (DNA and RNA) synthesis
ØInterfering with the transcription to inhibit RNA synthesis
ØInhibition of protein synthesis
ØInterfering with hormone balance

10
Mechanisms of Antineoplastic Drugs
Most antineoplastic drugs act on the proliferating
cycle of cell
(1)
destruction of DNA or inhibition of DNA
duplication
–
e.g. alkylating agents, mitomycin C
(2)
inhibition of nucleic acid (DNA and RNA)
synthesis
–
e.g. 5-fluorouracil, 6-mercaptopurine,
methotrexate, cytarabine, etc.

11
(3)
Interfering with the transcription to inhibit RNA
synthesis
–
e.g. dactinomycin, dauoruicin, and
doxorubicin
(4)
Inhibition of protein synthesis
–
e.g. vinca alkaloids, epipodophylotoxins, and
paclitaxel
(5)
Interfering with hormone balance
–
e.g. adrenal corticosteroids, estrogens,
tamoxifen etc.
Mechanisms of Antineoplastic Drugs

12
Cancer chemotherapy
n
Growth fraction
n
Proliferating cells , Non-proliferating cells
n
Mechanisms of Antineoplastic Drugs
n
Toxicity of Antineoplastic Drugs
n
Classification of Antineoplastic Drugs
n
Principles of combination therapies
Ødestruction of DNA or inhibition of DNA duplication
Øinhibition of nucleic acid (DNA and RNA) synthesis
ØInterfering with the transcription to inhibit RNA synthesis
ØInhibition of protein synthesis
ØInterfering with hormone balance

13
Toxicity of Antineoplastic Drugs
Short-term toxicity
n
Common side reactions usually appear
earlier and many of them occur in rapid-
proliferating tissues such as marrow,
gastrointestinal tract, and hair follicle.
n
myelosuppression,
n
gastrointestinal tract symptom
n
alopecia

14
Long-term toxicity
n
The long-term toxicity mainly occurs in
the patients who received
chemotherapy
many years ago.
n
Examples: carcinogenesis, teratogenesis
and sterility.
Toxicity of Antineoplastic Drugs

15
Cancer chemotherapy
n
Growth fraction
n
Proliferating cells , Non-proliferating cells
n
Mechanisms of Antineoplastic Drugs
n
Toxicity of Antineoplastic Drugs
n
Classification of Antineoplastic Drugs
n
Principles of combination therapies
phase of proliferation cycle
source and action mechanisms

16
Classification of Antineoplastic Drugs
n
On the basis of antineoplastic action on the phase
of proliferation cycle, drugs are classified as
n
cell cycle non-specific agents
(phase non-
specific agents,
CCNSA
)
(e.g. alkylating agents)
n
Act in all proliferating phases, even the G
0
n
effects are stronger.
n
cell cycle specific agents
(phase specific agents,
CCSA
). (e.g.
Antimetabolites, vinca alkaloids)
n
just act on specific phases of the cell cycle
n
effects are comparatively weaker.

17
n
On the basis of source and action
mechanisms, the drugs are also classified
as:
n
alkylating agents,
n
antimetabolites,
n
natural products,
n
hormones and antagonists
n
miscellaneous agents.
Classification of Antineoplastic Drugs

18
(Ⅰ) Alkylating Agents
n
Alkylating agents act via a reactive alkyl (R-
CH
2
-CH
2
+
-) group that reacts to form
covalent bonds with nucleic acids.
n
There follows either cross-linking of the two
strands of DNA, preventing replication, or
DNA breakage.
n
All alkylating agents are
phase
phase
-
-
nonspecific
nonspecific
.
n
kill rapidly proliferating cells, also kill non-
proliferating cells.

19
n
Examples: Mechlorethamine
n
the first drug
used in the treatment of cancer
n
At present, it is mainly used for
Hodgkin's disease
and non-Hodgkin's lymphomas.
n
Examples: Cyclophosphamide
n
Most widely used in clinical therapy for treatment
of cancer at present.
n
It has no antineoplastic action outside the body
and must
be activated in the liver
(
Ⅰ
) Alkylating Agents

20
(Ⅱ) Antimetabolites
n
Antimetabolites are analogues of normal
metabolites and act by competition, replacing
the natural metabolite and then subverting
cellular processes.
n
Examples of antimetabolites include:
n
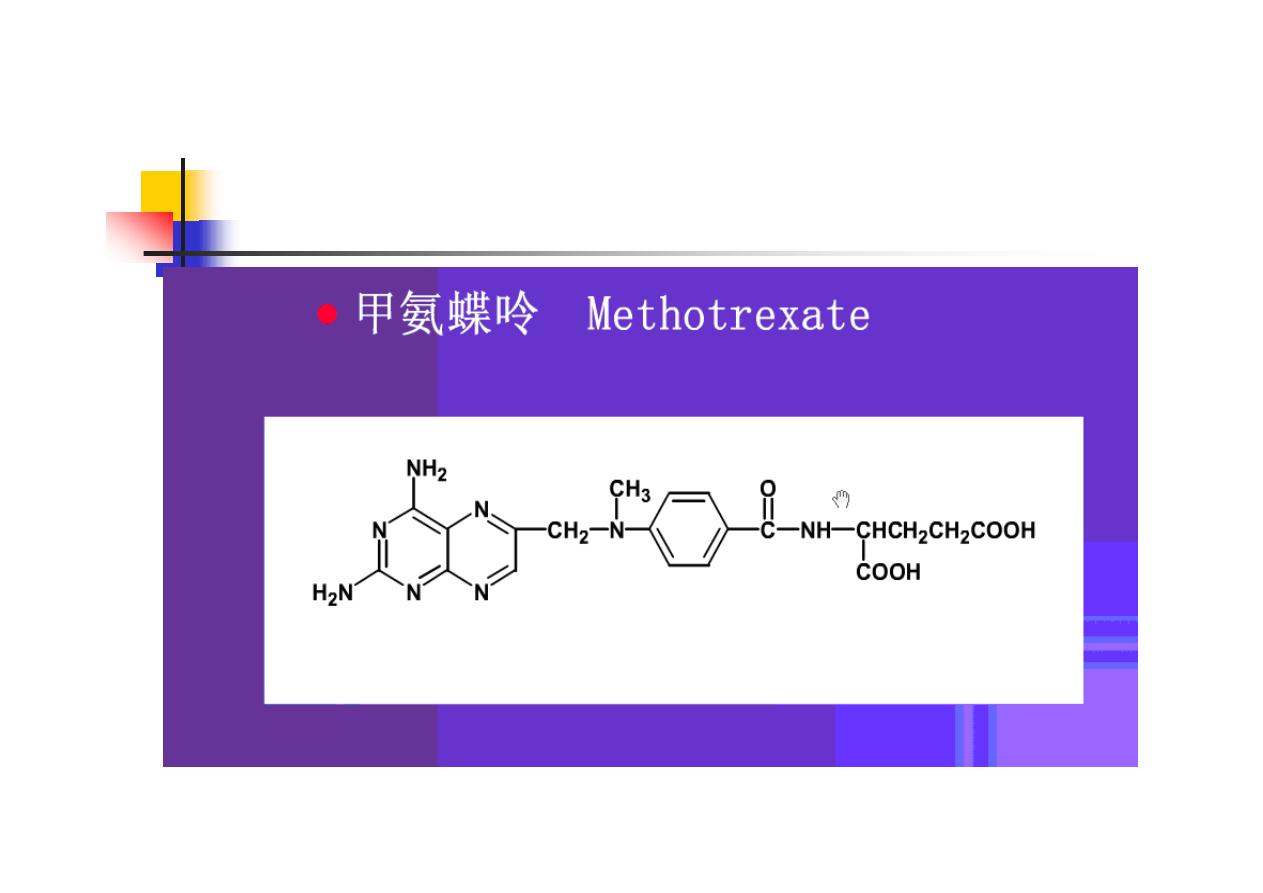
Folic acid antagonists (e.g. Methotrexate ).
n
Antipyrimidines (e.g. 5-Fluorouracil, Cytarabine).
n
Antipurines ( e.g. 6-Mercaptopurine )
21
(Ⅱ) Antimetabolites

22
(Ⅱ) Antimetabolites
n
Example: methotrexate
n
Mimics folic acid, which is needed for
synthesis of DNA, RNA and some amino
acids
n
It acts mainly on the
S phase cells
.
n
has a serious myelosuppression

23
(Ⅱ) Antimetabolites
n
Example: 6-Mercaptopurine
n
A structural analogue of hypoxanthin
n
It must be converted intracellularly to the
nucleotide 6-mercaptopurine ribose
phosphate and 6-methylmercaptopurine
ribonucleotide, and then
inhibit
purine
biosynthesis, causing inhibition of
biosynthesis of nucleic acid.
24
(Ⅱ) Antimetabolites

25
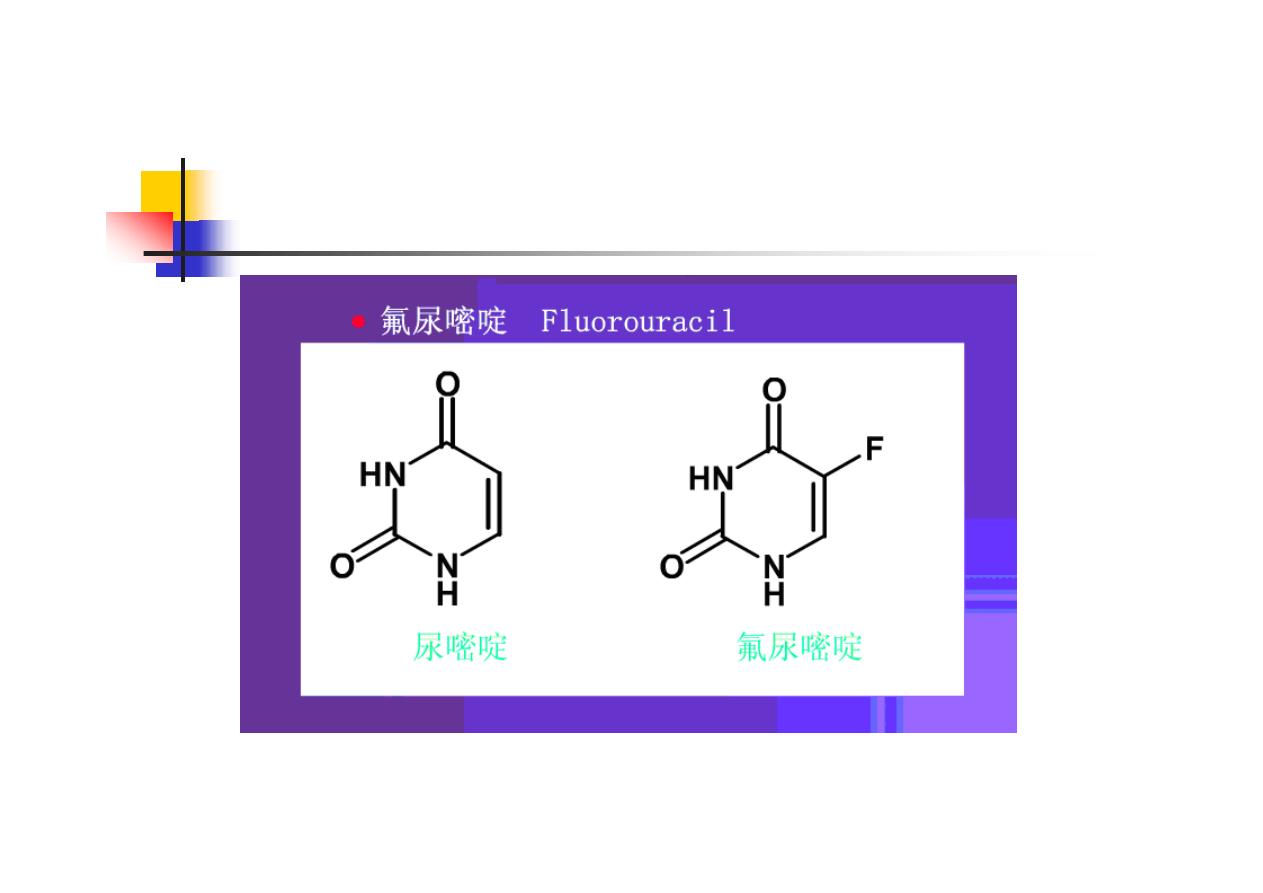
(Ⅱ) Antimetabolites
n
Example: 5-Fluorouracil (5-FU)
n
a flurorine-substituted analogue of uracil
n
must be metabolically activated to a
nucleotide, in this case FdUMP.
n
then its metabolite
inhibits
the synthetase
of deoxythymidine monophosphate,
blocking DNA synthesis. Besides, as the
fraudulent substance, its metabolite can
also interfere with the synthesis of RNA.
n
a phase-specific drug
.

26
(Ⅲ) Natural Products
n
This group is determined by the source of the
drug
n
The major classes of natural products include
n
antibiotics
n
vinca alkaloids
n
biologic response modifiers
n
enzymes
n
epipodophyllotoxins
n
taxanes

27
n
Antibiotic antineoplastic agents
n
Damage DNA in cycling and noncycling cells
n
Example:
Dactinomycin (actinomycin D)
This drug binds noncovalently to double-stranded
DNA
and inhibits
DNA-directed RNA syntheisis.
Dactinomycin is
a phase-nonspecific agent
,
but it is more active agsinst G1 phase cells.
(Ⅲ) Natural Products

28
(Ⅲ) Natural Products
n
Vinca (plant) alkaloids
n
Vincristine and vinblastine are alkaloids
derived from the periwinkle plant.
n
binding to tubulin, interfere with the
assembly of spindle proteins during
mitosis..
n
Act in
M phase
to inhibit mitosis, blocking
proliferating cells as they enter metaphase.
n
Both can cause bone marrow suppression
and neurotoxicity

29
(
Ⅳ
) Hormones and antagonists
n
The growth of some cancers is hormone
dependent. Growth of such cancers can
be inhibited by surgical removal of
hormone glands, increasingly, however,
administration of hormones or
antihormones is preferred.

30
Examples:
n
Adrenocortical steroids to
inhibit the
growth
of cancers of
lymphoid
tissue
and blood.
n
Oestrogen antagonists ( tamoxifen ) is
indicated for breast cancer.
n
Oestrogen is used for prostatic cancers.
(Ⅳ) Hormones and antagonists

31
(Ⅴ) Miscellaneous agents
n
Examples: Hydroxyurea
n
Hydroxyurea inhibits ribonucleotide
reductase. inhibition of DNA synthesis.
n
It is specific for the cells of
S
phase
n
The major adverse effect of this drug is
bone marrow depression.
32
Cancer chemotherapy
n
Growth fraction
n
Proliferating cells , Non-proliferating cells
n
Mechanisms of Antineoplastic Drugs
n
Toxicity of Antineoplastic Drugs
n
Classification of Antineoplastic Drugs
n
Principles of combination therapies
1. Select drugs according to their phase specific characteristics
2. Combinations of antineoplastic drugs with different action mechanism
3. Combinations of antineoplastic drugs with other therapies
5. Select drugs according to antineoplastic range (spectrum)
6. Use right dose

Principles of combination therapies
n
In order to
enhance curative effect
, to
decrease the toxicity and to reduce the drug
resistance, combination therapies are often
used in the treatment.
n
Advantages of drug combinations:
n
They provide maximal
cell kill
within the range of
tolerated toxicity.
n
They are effective against a broader range of cell-
cycle phases.
n
They may slow or prevent the development of
resistance.

34
1.
Select drugs according to their phase
specific characteristics
The aim of this rule is to urge more G
0
phase
cells to enter the proliferating cycle so as to
increase
the amount of tumor cells killed by
drugs.
Principles of combination therapies

35
– For
high GF tumor
such as acute leukemia,
phase specific drugs are firstly used to kill S
or M phase cells, and then phase non-speicfic
drugs are used to kill tumor cells in other
phases, and finally the above two steps are
repeated once again to kill new cell from G
0
phase.
– For
low GF tumor
such as solid tumors, phase
non-specific drugs are firstly used to kill cells
of all phases, and then phase specific drugs
are used, and finally the above steps are
repeated to kill the new cell from G0 phses.
Principles of combination therapies

36
2. Combinations of antineoplastic drugs with
different action mechanisms.
can destroy tumor cells from various biochemical links
at same time.
3. Combinations of antineoplastic drugs with other
therapies
Examples: chemotherapy plus operation,
chemotherapy plus radiotherapy.
Principles of combination therapies

37
4. Combination of low-toxic drugs with high-
toxic ones
does not obviously increase the toxicity of
antineoplastic drugs while the remarkable
synergism of anticancer action is produced.
Example: bleomycin (light myelosuppression)
+ mitomycin (serious myelosuppression),
which is often used to treat carcinoma of
cervix.
Principles of combination therapies

38
5. Select drugs according to antineoplastic
range (spectrum)
6. Use right dose
Principles of combination therapies
39
Cancer chemotherapy
n
Growth fraction
n
Proliferating cells , Non-proliferating cells
n
Mechanisms of Antineoplastic Drugs
n
Toxicity of Antineoplastic Drugs
n
Classification of Antineoplastic Drugs
n
Principles of combination therapies
1. Select drugs according to their phase specific characteristics
2. Combinations of antineoplastic drugs with different action mechanism
3. Combinations of antineoplastic drugs with other therapies
5. Select drugs according to antineoplastic range (spectrum)
6. Use right dose

Thank you!!
