1
Dr. Yasameen Alsaffar
Lec 2
THE HYPOTHALAMUS AND THE PITUITARY GLAND
Functional anatomy:
The pituitary gland is enclosed in the sella turcica and bridged over by a fold of
dura mater called the diaphragma sellae, with the sphenoidal air sinuses below
and the optic chiasm above. The cavernous sinuses are lateral to the pituitary
fossa and contain the 3rd, 4th and 6th cranial nerves and the internal carotid
arteries. The gland is composed of two lobes, anterior and posterior, and is
connected to the hypothalamus by the infundibular stalk, which has portal
vessels carrying blood from the median eminence of the hypothalamus to the
anterior lobe and nerve fibers to the posterior lobe.
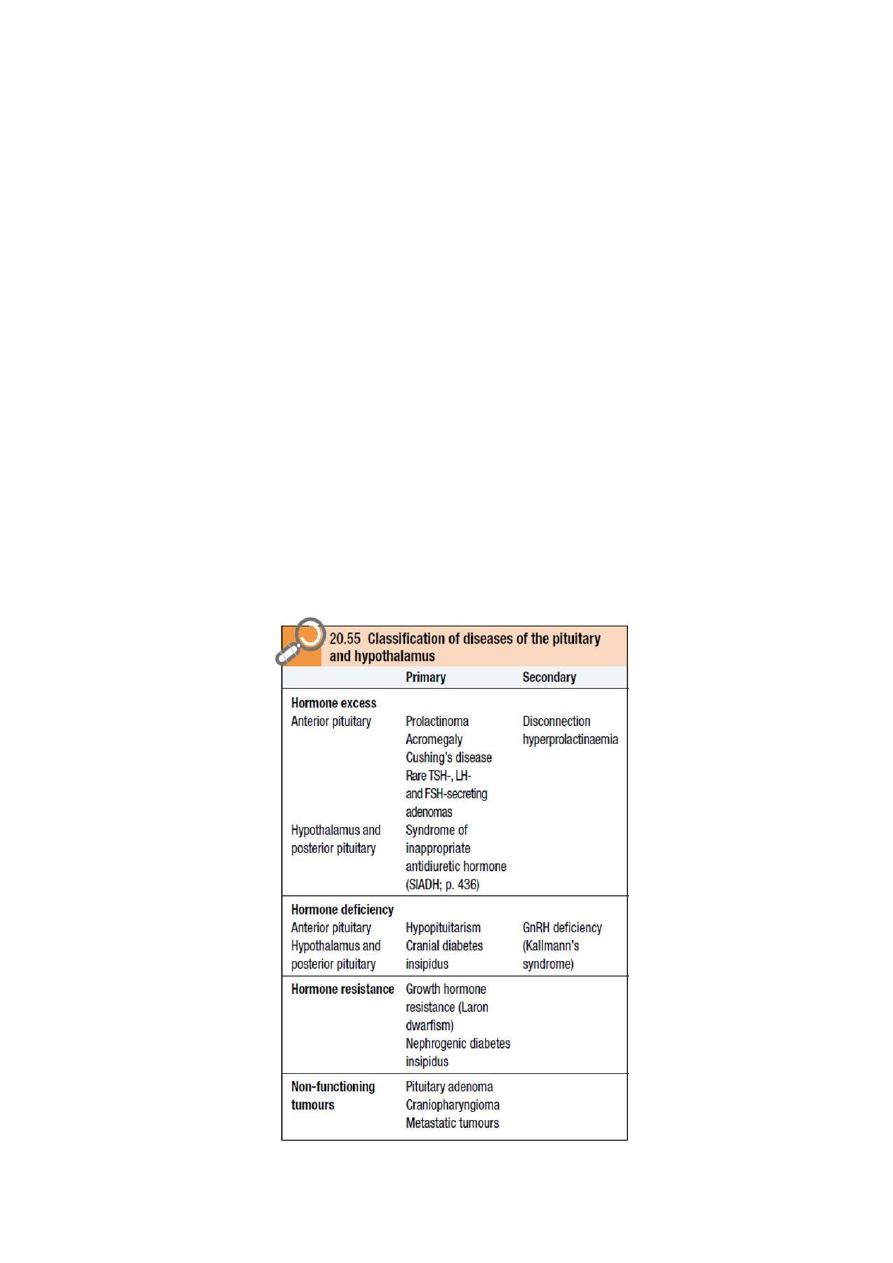
Classification of diseases of the pituitary and hypothalamus

2
Hypopituitarism
Hypopituitarism describes combined deficiency of any of the anterior pituitary
hormones. The clinical presentation is variable and depends on the underlying
lesion and the pattern of resulting hormone deficiency.
Causes:
A- Structural:
1- Primary pituitary tumour: Adenoma
2- Craniopharyngioma
3- Secondary tumour (including leukaemia and lymphoma)
4- Meningioma.
5- Haemorrhage (apoplexy)
B- Inflammatory/infiltrative
1- Sarcoidosis
2- Infections, e.g. pituitary abscess, tuberculosis, syphilis, encephalitis
3- Haemochromatosis
C- Congenital deficiencies
E.g.: GnRH (Kallmann’s syndrome)
D- Functional
1- Chronic systemic illness
2- Anorexia nervosa
3- Excessive exercise
E- Other
1- Head injury
2- (Para)sellar surgery
3- (Para)sellar radiotherapy
4- Post-partum necrosis (Sheehan’s syndrome)
Clinical assessment:
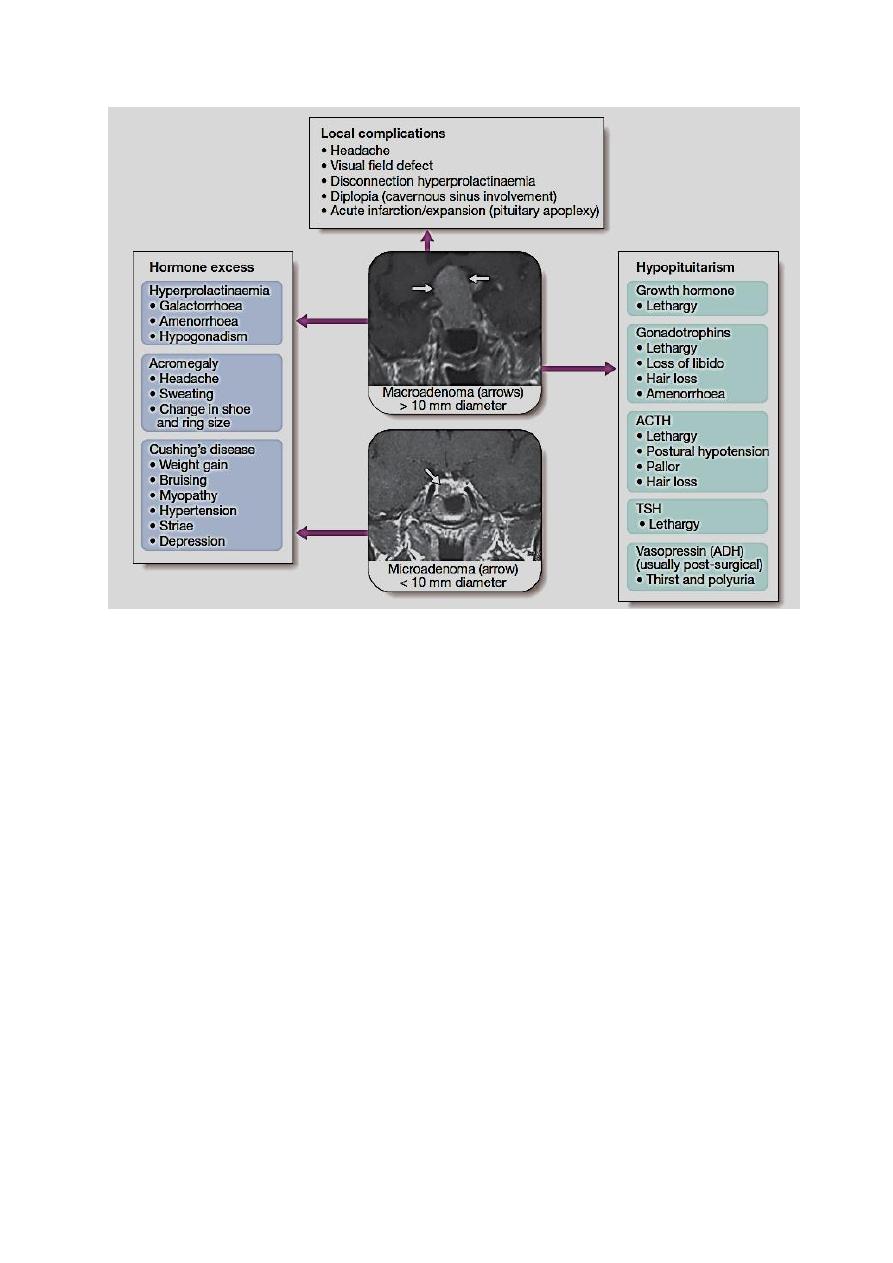
The clinical feature of hypopituitarism related to hormonal deficiency, with
feature of the cause either hormonal or local effect, for example patient with
functional adenoma had feature of the hormonal released by adenoma and
feature of local compression on the surrounding, in addition to the feature of the
hormonal deficiency of the rest of other hormone and as shown in the following
figure:
3
The onset of hormonal deficiency varies according to type of hormone, the first
hormone to be lost is growth hormone (which had nonspecific symptom such as
lethargy, muscle weakness and increased fat mass), this followed by LH and
FSH, and followed by ACTH, and the last hormone to be lost is TSH.
(Don’t forget: grow flat).
The onset of all of the above symptoms is notoriously insidious. However,
patients sometimes present acutely unwell with glucocorticoid deficiency. This
may be precipitated by a mild infection or injury, or may occur secondary to
pituitary apoplexy.
Investigation:
ACTH deficiency:
Short ACTH stimulation test
Insulin tolerance test: only if there is uncertainty in interpretation of short
ACTH stimulation test (e.g. acute presentation).
LH/FSH deficiency:
In the male, measure random serum testosterone, LH and FSH •

4
In the pre-menopausal female, ask if the menses are regular •
In the post-menopausal female, measure random serum LH and FSH
(FSH normally > 30 IU/L and LH > 20 IU/L).
TSH deficiency:
Measure random serum T4. Note that TSH is often detectable
in secondary hypothyroidism.
Growth hormone deficiency
Only investigate if growth hormone replacement therapy is
being contemplated •
Measure immediately after exercise •
Consider other stimulatory tests arginine, glucagon and
clonidine.
Cranial diabetes insipidus
Only investigate if patient complains of polyuria/polydipsia, which
may be masked by ACTH or TSH deficiency •
Exclude other causes of polyuria with blood glucose, potassium and
calcium measurements •
Water deprivation test or 5% saline infusion test Identify hormone
excess •
Others
Measure random serum prolactin •
If there are clinical features establish the anatomy and diagnosis
consider visual field testing •
Image the pituitary and hypothalamus by MRI or CT
Management:
Firstly we have to treat the cause.
In acute presentation we treat like that of adrenocortical insufficiency except
that sodium depletion is not an important component to correct. Chronic
hormone replacement therapies include:

5
Cortisol replacement
Hydrocortisone should be given if there is ACTH deficiency.
Mineralocorticoid replacement is not required.
Thyroid hormone replacement
Levothyroxine 50–150 μg once daily should be given. Unlike in primary
hypothyroidism, measuring TSH is not helpful in adjusting the replacement
dose because patients with hypopituitarism often secrete glycoproteins which
are measured in the TSH assays but are not bioactive. The aim is to maintain
serum T4 in the upper part of the reference range. It is dangerous to give thyroid
replacement in adrenal insufficiency without first giving glucocorticoid therapy,
since this may precipitate adrenal crisis.
Sex hormone replacement
This is indicated if there is gonadotrophin deficiency in women under the age of
50 and in men to restore normal sexual function and to prevent osteoporosis.
Growth hormone replacement
Growth hormone (GH) is administered by daily subcutaneous self-injection to
children and adolescents with GH deficiency and, until recently, was
discontinued once the epiphyses had fused.
Some individuals remain lethargic and unwell in spite of treatment of other
hormone.
These patients may feel better, and have objective improvements in their fat:
muscle mass ratios and other metabolic parameters, if they are also given GH
replacement. Treatment with GH may also help young adults to achieve a
higher peak bone mineral density. The principal side-effect is sodium retention,
manifest as peripheral oedema or carpal tunnel syndrome.
Pituitary tumour
Pituitary tumours produce a variety of mass effects, depending on their size and
location, most intrasellar tumours are pituitary macroadenomas (most
commonly nonfunctioning adenomas), whereas suprasellar masses may be
craniopharyngiomas. The most common cause of a parasellar mass is a
meningioma.

6
Clinical feature:
Common but non-specific presentation is with headache, which may be the
consequence of stretching of the diaphragm sellae. Although the classical
abnormalities associated with compression of the optic chiasma are bitemporal
hemianopia or upper quadrantanopia, any type of visual field defect can result.
Lateral extension of a sellar mass into the cavernous sinus with subsequent
compression of the 3rd, 4th or 6th cranial nerve may cause diplopia.
Occasionally, pituitary tumours infarct or there is bleeding into cystic lesions.
This is termed ‘pituitary apoplexy’ and may result in sudden expansion with
local compression symptoms and acute-onset hypopituitarism. Non-
haemorrhagic infarction can also occur in a normal pituitary gland; predisposing
factors include catastrophic obstetric haemorrhage (Sheehan’s syndrome),
diabetes mellitus and raised intracranial pressure.
Investigations
Patients suspected of having a pituitary tumour should undergo MRI or CT.
The definitive diagnosis is made on histology after surgery.
All patients with (para)sellar space-occupying lesions should have pituitary
function test.
Treatment:
The treatment of pituitary tumor by surgery as first line and radiotherapy as
second line and no role for medical treatment except in prolactinoma where the
medical treatment (dopamine agonist) regard as first line, and in acromegaly as
second line of treatment.
Urgent treatment is required if there is evidence of pressure on visual pathways,
in which surgery is needed except if the prolactin is over 5000 mU/L, then the
lesion is likely to be a macroprolactinoma and to respond to a dopamine agonist
with shrinkage of the lesion, making surgery unnecessary.
All operations on the pituitary carry a risk of damaging normal endocrine
function; this risk increases with the size of the primary lesion. Pituitary
function should be retested 4–6 weeks following surgery, primarily to detect the
development of any new hormone deficits.
Following surgery, usually after 3–6 months, imaging should be repeated and, if
there is a significant residual mass and the histology confirms an anterior
pituitary tumor, external radiotherapy may be given to reduce the risk of
recurrence. Radiotherapy is not useful in patients requiring urgent therapy
because it takes many months or years to be effective and there is a risk of acute
swelling of the mass.

7
Fractionated radiotherapy carries a life-long risk of hypopituitarism (50–70% in
the first 10 years) and annual pituitary function tests are obligatory. There is
also concern that radiotherapy might impair cognitive function, cause vascular
changes and even induce primary brain tumors.
Stereotactic radiosurgery, best delivered by the ‘gamma knife’, allows specific
targeting of residual disease in a more focused fashion.
Non-functioning tumours should be followed up by repeated imaging.
With best regard
