
1
Dr.Mohammed Qasim Mal-Allah
Pharmacology
Narcotic
Analgesics
“opioids”
Dr.Mohammed Q.Mal-Allah
Lec.1

2
Dr.Mohammed Qasim Mal-Allah
Analgesic:
is the drug that relieves pain, they are divided into two types:
1. Narcotic: which act centrally as Opioids.
2. Non-narcotic: they act peripherally as Aspirin.
Narcotics:
they relieve pain and also cause drowsiness and sedation. The
prototype drug is (Morphine) derived from Opium.
Opioids:
they are natural or synthetic compounds that produce morphine-like
action. They act on the CNS causing drowsiness and sedation.
Opiates:
this term refers to drugs as morphine or codeine that are obtained from
the juice of the opium poppy (they are natural). All of them act by binding to
specific receptors called (Opioid receptor) and produce effects that mimic the
action of endogenous peptides neurotransmitters (endorphines, dynorphine, and
enkephalines).
More recently the endogenous peptides (endomorphine-1 & endomorphine-2) have
been found to possess many of the properties of opioid peptides,
1
notably analgesia
and
2
high affinity biding to µ receptors.
Opioid Receptors:
The major effects of opioids are mediated by 4 families of receptors which
are: µ, Kappa, Delta, and Sigma.
Each of these receptors exhibit different specificity for the drug that they
bind.
Opioid drugs may be agonist to a receptor or antagonist or partial agonist or
mixed agonist-antagonist (act as agonist on some and antagonist on others).
This will lead to limited ceiling of therapeutic efficacy.

3
Dr.Mohammed Qasim Mal-Allah
Note: morphine is a full agonist, if you replace morphine by another drug such as
codeine (a weak agonist or a mixed agonist-antagonist), the patient will have
withdrawal syndrome.
Mode of Action:
All opioids receptors are coupled to inhibitory G-protein that cause inhibition of
adenylate cyclase, they may be associated with ion channels to increase K+ efflux
(hyper polarization) or decrease Cat influx thus impeding neuronal firing and
transmitter release.
At the level of spinal cord:
In the pre-synaptic terminal we have µ, δ, and K receptors, so opioids
action on these receptors will cause decrease Ca
+
influx and decrease
transmitter release e.g. ACh, Noradrenaline, Glutamate, Substance P, and
others.
While at the post-synaptic neuron we have µ receptors, so opioids will
cause increase K
+
efflux (hyperpolarization).
At the Supra Spinal level:
Opioids either directly inhibit these neurons or on the other hand neurons
that send processes to the spinal cord and inhibit pain, transmission neurons
are activated. This activation results from the inhibition of the pain
inhibitory neurons at several locations.
Opioids inhibit the inhibitory (GABAnergic) inter-neuron; the pain
inhibitory neuron will be indirectly excited by opioids.
Under most circumstances opioids concurrently act on both spinal and supra
spinal sites and interaction at these two sites tend to increase the overall
analgesic efficacy. Different combination of opioids receptors are found in

4
Dr.Mohammed Qasim Mal-Allah
the spinal and supra spinal sites implicated in pain transmission when
opioids directly inhibit the neurons or indirectly inhibit them.
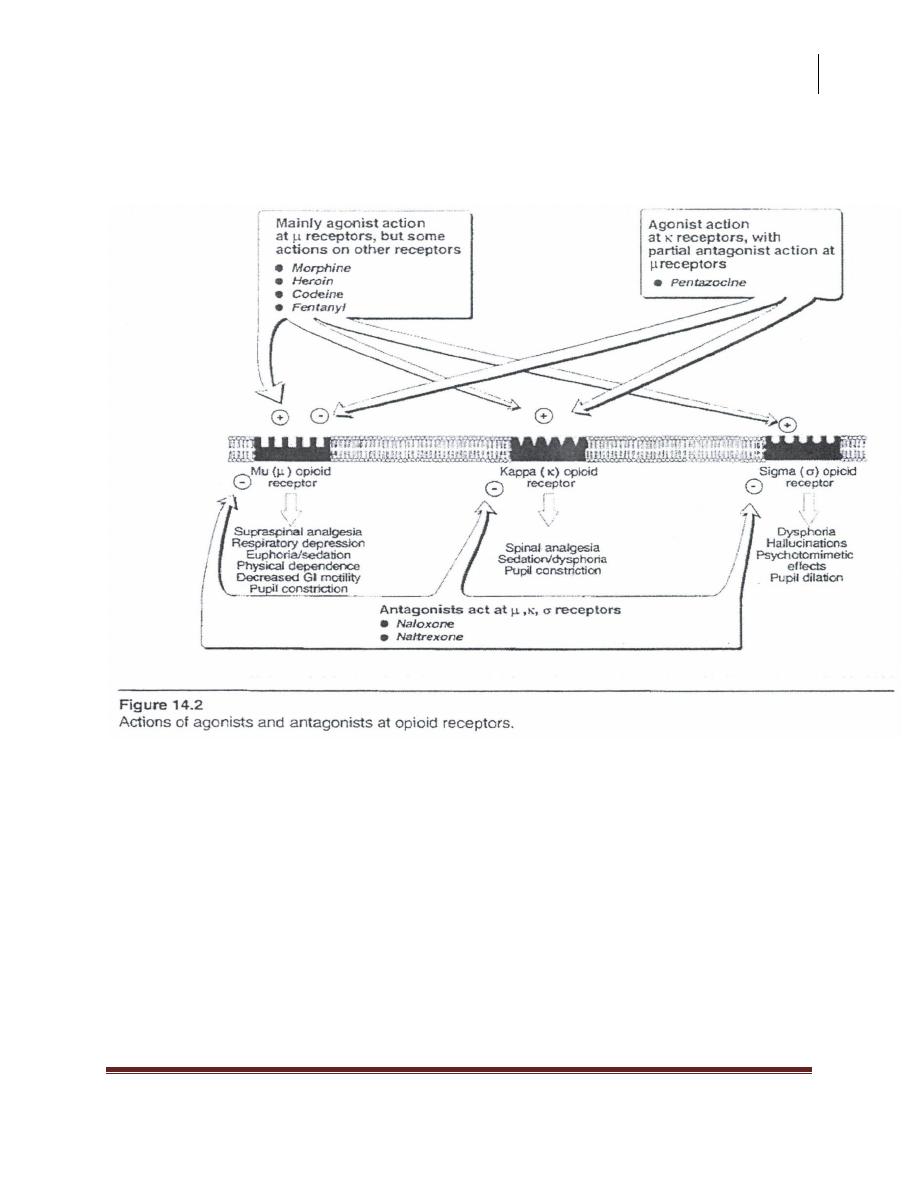
Actions of opioids receptors:
1.Mu (µ) receptor:
They mediate spinal and supra spinal analgesic, miosis, respiratory depression,
euphoria, sedation, physical dependence, decrease GIT motility and they modulate
neurotransmitter and hormonal release.
There are subtypes of µ receptors which are µ
1
, µ
2
.
Endorphines > enkephalines > dynorphines.
2.Kappa (K) receptor:
They mediate spinal and supra spinal analgesia, miosis, dysphoria, slowed GIT
trans.
Dynorphin » endorphin and enkephalin
3.Delta (δ) receptor:
Their function is not well defined, they are present in the limbic system and they
may be involved in changes in the effective behavior.
enkephaline bind more selectively with delta receptors » endorphin and
dynorphin.
Delta receptors also mediate supra spinal and spinal analgesia and cause
modulation of hormone and neurotransmitter release.
4.Sigma (σ) receptor:
They are less specific because they may bind to non-opioid agents e.g.
phencyclicidine "a hallucinogen". They mediate dysphoria, hallucination,
respiratory stimulation, and pupil dilation .
5
Dr.Mohammed Qasim Mal-Allah
δ and µ are also found in the nerve plexuses and endocrine gland of
intestine.
Distribution of opioid receptors:
High density of opioid receptors are present in 5 general areas in the CNS known
to be involved in the integration of information about pain, these descend from the
peri-aquiductal gray matter (PAG) through the dorsal horn of the spinal cord. They
are also found in the periphery.
1. Brain stem: the opioid receptor mediate the following: respiration, cough,
nausea, vomiting, Maintenance of blood pressure, pupil diameter, and control the
stomach secretions.
Nucleus of tractus solitarius and related nuclei are involved in vagal refluxes.

6
Dr.Mohammed Qasim Mal-Allah
2. Medial thalamus: here, the receptors mediate the deep pain that is poorly
localized and emotionally influenced.
3. Spinal Cord: through substantia gelatinosa which is concerned with receiving
and integration of incoming sensory information.
4. Limbic System: high density of receptors is found in amygdala. This area
influence emotional behavior (emotional reaction to pain).
5. Hypothalamus: the receptors effect neuroendocrine secretions.
6. The Periphery: they bind to peripheral sensory nerve plexuses and their
terminals. They inhibit Ca
+
dependent release of excitatory pro inflammatory
substances (substance P) from these nerve-endings which may contribute to the
anti-inflammatory and analgesic effect of opioids.
7. The Immune Cells: the function is not well-defined.
Endogenous Opioids and their Precursors:
These are peptides act as neurotransmitters, found in the complex pain inhibitory
system. They include:
1. Enkephalines: (methione enkephaline and leucine enkephaline) they are
derived from preproenkephaline i.e. proenkephaline-A.
2. Dynorphines A and B: they are derived from preprodynorphine, i.e.
proenkephaline-B.
3. Endorphines: Especially S-endorphine, derived from Qro-
Qpiomelano~ortin (POM C} that gives ACTH, MSH, and BLPH –> β-
endorphine.

7
Dr.Mohammed Qasim Mal-Allah
Summary of opioid analgesics and antagonists,
The mixed agonist antagonist were developed to eliminate the potential for
abuse while retaining the analgesic effect and they cause less dependence
and less respiratory depression but cause (withdrawal syndrome) in addicts
on morphine (the prototype).

8
Dr.Mohammed Qasim Mal-Allah
Morphine
It has the following actions:
1)) CNS:
Depressant, stimulant, euphoria, dysphoria, dependence.
Depressant actions:
1. Analgesia: by increasing spinal and supraspinal pain threshold at the spinal
cord level and altering the brain perception of pain, so the pain is felt but the
sensation is no more unpleasant.
2. Drowsiness and mental clouding, so it has useful hypnotic and tranquilizer
effect.
3. Respiratory effect: decrease the rate and depth by decreasing the sensitivity
of the respiratory center to raised CO
2
tension in blood.
* Therapeutic dose --> decrease minute volume due to decreased rate and tidal
volume.
* Higher dose --> CO
2
narcosis
* Over dose --> respiratory arrest
* morphine is dangerous in patients with chronic obstruction, pulmonary disease,
and asthma, in which it will also increase the viscosity of bronchial secretions in
addition to bronchospasm due to histamine release.
4. Inhibition of cough center: cough suppression, the receptors involved may
be different than those involved in analgesic effect.
5. Increase the intracranial pressure: due to CO2 retention, dilation of
cerebral vessels, and increase the CSF pressure, therefore --> morphine is
contraindicated in patients with severe head injury.
6. Polysynaptic refluxes: in the spinal cord are inhibited.

9
Dr.Mohammed Qasim Mal-Allah
7. Hormonal decrease in GnRH, CRH -7 decreases LH and FSH, and also
decrease ACTH -7 decrease in Bendorphine and cortisol.
Stimulatory actions:
1. Miosis, pin point pupil is characteristic of morphine poisoning and use as a
result of stimulation of mu and kappa receptors.
Morphine stimulates 3
rd
nerve nucleus which cause enhancement of the
parasympathetic stimulation to the eye and thus miosis.
There is only little tolerance to this effect (even addicts show pin point pupil)
* This is an important diagnostic feature of coma because most other causes of
coma cause dilation of the pupil.
2. Emesis, 40% nausea, and 10% vomiting, this is caused by direct stimulation
to the chemoreceptor trigger zone.
3. Monosynaptic spinal cord refluxes are stimulated leading to straub tail in
animals; also it causes trunkal rigidity and myoclonus in man.
Morphine is not used in case of tetanus or convulsant poisoning; indeed morphine
itself can cause convulsions.
4. Rarely, excitation in some animals as cats and horses.
5. Release of ADH, prolactin, and GH by diminished dopaminergic inhibition.
2)) on smooth muscles:
a. GIT opioidreceptors exist in increased density in GIT.
In the small intestine, resting tone is increased with periodic spasms, but the
amplitude of segmental non-propulsive contractions is decreased, it causes
spasm of sphincters.

10
Dr.Mohammed Qasim Mal-Allah
In the large intestine, it decreases propulsive contractions, peristalsis, and
tone is increased. It decreases intestinal secretions.
In the stomach, it delays gastric emptying, decreases motility and HCI
secretion.
It causes constipation due to increased transient time and it increases
viscosity of feces due to increased water absorption.
Central action of these drugs leads to neglection of the urge to defecate and
contribute to constipation.
Morphine increases the intrasigmoidal pressure; therefore it is
contraindicated in patients with (diverticularis disease).
Pethidine does not produce this high pressure and it can be used if needed.
Morphine endangers the intestinal anastamosis and should note used in
intestinal obstruction.
b. Biliary system:
1. Spasm of sphincter of oddi --> increases intrabiliary pressure.
2. Sometimes, biliary colic is worsened by morphine if the dose is enough only
to cause increased intrabiliary pressure with only slight analgesia.
This effect can be reversed by naloxone or GTN (glyceryl trinitrate), but it is not
effectively reversed by atropine.
3. Because of the increase in the intrabiliary pressure by morphine, this may
tend to damming back of the pancreatic juice and so cause increase in the
serum amylase level. Therefore, it is best avoided in patients with
pancreatitis.
c. The bronchi:
They are constricted (i.e. spasm).

11
Dr.Mohammed Qasim Mal-Allah
d. Ureter: spasm.
e. Bladder.
Spasm of the sphincter that leads to retention of urine in patients with benign
prostatic hyperplasia.
f. Uterus:
Labor is prolonged due to slowing of the effective contraction --> prolong child
birth.
g. CVS: by central action morphine impairs sympathetic responses (vascular)
causing veno and arteriolo dilation and stimulates the vagal center -7 bradycardia
(this effect can be blocked by atropine).
Also it causes release of histamine --> vasodilation; arteriolar dilation may cause
hypotension in patients with acute M.1. In the normal persons these effects on CVS
are not so important, but can benefit patients with acute left ventricular failure
(acute pulmonary edema) due to the following effects:
a. Mental distress --> by tranquilizer effect.
b. Cardiac distress --> by decreasing the sympathetic drive
c. Respiratory distress --> by rendering the respiratory center insensitive to
afferent stimuli coming from the conjusted lungs.
Pharmacokinetics:
1. Absorption from GIT is slow and erotic.
2. Oral is double the injection dose.
3. It undergoes significant 1st pass elimination, therefore it is usually given
I.M. or LV. or S.C., also given in buccal and sublingual routes in which the
dose is equal to that of the I.M. route, and it is given as transdermal patch.
4. It is also taken by inhalation of crude opioid for the non-medical purposes -7
rapid onset of action.

12
Dr.Mohammed Qasim Mal-Allah
5. Morphine enters all the tissues and can cross the placenta causing respiratory
depression in the fetus at birth.
6. T1/2 = 2hrs, duration of action = 4-6 hrs.
7. It is metabolized in liver and kidney to the followings:
morphine-6-glucoronide --> active
morphine-3-glucoronide --> inactive
8. Conjugated morphine is excreted in the urine and small amount appears in
the bile.
Clinical Uses:
1. Relief of severe pain, which is either visceral (M.I.) or somatic (as wounds,
fractures). (distinguish between morphine and aspirin which is used only in
mild and moderate somatic pains)
2. Relief of anxiety in serious and frightening diseases accompanied by pain,
e.g. accidents or hemorrhage (in this case morphine should be given after
replacement of fluid loss).
3. Relief of dyspnea in acute left ventricular failure.
4. Production of euphoria and relief pain of dying.
5. Premedication for surgery, application in anesthesia (general or local
anesthesia).
6. Symptomatic control of non-serious diarrhea e.g. traveler’s diarrhea
(codeine, loperamide).
7. Suppression of cough (morphine-like substance) codeine.
8. To control acute restlessness (rarely).

13
Dr.Mohammed Qasim Mal-Allah
Adverse Effects:
a. Respiratory depression.
b. Vomiting.
c. Dysphoria.
d. Hypotension.
e. Retention of urine in (BPH).
f. Pruritis (itching around the nose).
Contraindications:
1. CNS:
I.
Head injury because it increases intracranial pressure.
II.
Acute alcoholism.
III.
Convulsion disorders.
2. Respiratory system: in asthma and chronic obstructive pulmonary disease
(COPO).
3. GIT:
I.
Diverticulitis.
II.
Pancreatitis.
III.
Biliary infections.
IV.
Intestinal anastamosis resection and obstruction.
4. In severe liver disease (acute or chronic) that leads to toxic effects
(enkephalopathy).

14
Dr.Mohammed Qasim Mal-Allah
5. Avoided during labor.
6. Patients with adrenal insufficiency and myxedema i.e. hypothyroidism may
experience extended effect from opioids.
Morphine interaction:-
a. Phenothiazine: enhances depressant effect of morphine.
b. Tricyclic antidepressants.
c. Sedative hypnotics: they increase eNS depressant & respiratory depression.
d. MAO inhibitors: result in hyperpyrexia & hypertension.
e. Amphetamine: in low doses they enhance analgesia.
Tolerance & physical dependence:
Repeated use leads to tolerance, along with tolerance, dependence also
developed.
Tolerance occurs mainly to the agonist effects which are respiratory
depression, analgesia, euphoria & sedative effects, but not to the stimulatory
actions as miosis & constipations & convulsions.
Also tolerance occurs to nausea & vomiting & to anti-diuresis.
There is cross tolerance between opioids & with other CNS depressants as
barbiturates & alcohol drugs with mixed agonist & antagonist actions
produce tolerance to the agonist actions only.
If tolerance is prevented, physical dependence is also prevented.
Physical & psychological dependence occur readily with morphine & other
drugs that produce autonomic, motor & psychological responses that
incapacitate the individual with severe, unbearable symptoms, however they

15
Dr.Mohammed Qasim Mal-Allah
rarely cause death. The mechanism of tolerance & dependence is poorly
understood.
Chronic exposure to opioids leads to adaptive changes in the endogenous
opioid system & in the receptor no. & sensitivity & in the cellular responses,
thus the abrupt withdrawal of the administration of the opioid would be
expected to produce rebound or withdrawal syndrome.
Withdrawal syndrome consists largely from the opposite actions of opioids,
also noradrenalin mechanism is modulated by the continuous opioid
administration, and so abrupt withdrawal will lead to noradrenergic storm.
Treatment of addicts:
1. Withdraw morphine gradually.
2. Substitute methadone which produces mild withdrawal syndrome, since it
has long t1/2 (48hrs), perhaps supplements with chlorpromazine or
benzodiazepine as valium.
3. Clonidine decreases the severity of withdrawal syndrome by decreasing the
effects of noradrenalin hyperactivity. (Clonidine stimulates presynaptic α2 –
R --> inhibition of the sympathetic over activity).
* Lofexidine is clonidine analogue that may also aid opioid detoxification.
* Sometimes, we also use atropine or Beta blockers as propranolol that decreases
emotional compulsions after stopping opioid.
Tolerance to opioids:
On exposure to opioids, the body will be adapted by:
1. Change in the number of opioid receptors.

16
Dr.Mohammed Qasim Mal-Allah
2. Change in the sensitivity of these receptors, or more recently is due to a
structural dysfunctional interaction between receptors & the G protein
secondary messenger system.
Morphine Poisoning:
Coma, slow & shallow respiration, pinpoint pupil, circulation is maintained till
hypoxia is advanced & cyanosis occurs. The main signs of morphine poisoning
are:
1. Bradypnea.
2. Patient coma in an unconscious state & pupils are constricted (miosis), while
in most other cases of coma the pupil is dilated.
Treatment of morphine poisoning:
1. Support of respiration & circulation till antagonize the effect of opioids.
2. We give naloxone I.V.-7 it's a pure opioid antagonist, also it is used as a test
(therapeutic test) whether the coma is due morphine or not, by giving
naloxone.
Individual opioids: they're classified into:
I. High efficacy opioids:
a. Morphine
b. Pethid ine
c. Methadone
d. Diamorphine (heroin).

17
Dr.Mohammed Qasim Mal-Allah
e. Fentanyl
A.
Morphine:
mentioned before.
B.
Pethidine
(demerol, meperidine): it is commonly used, has less efficacy
than morphine, but it is effective in pain beyond reached of codeine. It is like
morphine in causing respiratory depression, euphoria & vomiting.
Structurally, it is not related to morphine, but it shares many properties with
morphine including that of being antagonized by naloxone.
Pethidine differs from morphine by (important):
1. Act by binding to Kappa receptors rather than µ.
2. Doesn't suppress cough usefully.
3. Causes less intense & less frequent constipation.
4. It less likely to prolong child-birth so is used in 1
st
stage of labor.
5. Little hypnotic effect & the period of analgesic effect are shorter than
morphine (2-3 hrs.).
6. It has atropine like effects: dry mouth, blurred vision {(cycloplasia) &
sometimes mydriasis though usually miosis}.
7. By using pethidine can't have pin -point eye (pupil) because of atropine like
effect.
8. Overdose leads to myoclonus & convulsions (both may occur in renal failure
--> pethidine not excreted --> high concentration).
9. Dependence is less marked than morphine.
Clinical uses of pethidine:

18
Dr.Mohammed Qasim Mal-Allah
1. Relieve severe pain like post-operative pain.
2. Dyspnea of acute left ventricular failure.
3. Pre-operative medication.
4. I.V. to reduce dislocations & fractures.
Pethidine tl/2 is 3hrs, oral dose is 50-100 mg (also can be given as injection),
metabolized to "norpethidine" which can cause excitement & convulsions in
pethidine poisoning.
C.
Methadone:
it is a synthetic drug structurally related or similar to
morphine & acts mainly on µ receptors. The analgesic activity is equal to
that of morphine & very effective orally.
It causes less sedation & less euphoria than morphine.
Vomiting is common, but again less than morphine.
It increases the intrabiliary pressure & increases constipation.
t1/2 is 48hrs.
Analgesia lasts for 24 hrs.
Dependence occurs, but is less severe & causes less severe withdrawal
syndrome because of long tl/2, therefore the addicts on morphine & heroin
are transported to methadone as one step of treatment.
It is useful for cough:- suppresses cough carefully.
Main uses: 1. analgesia 2. Cough suppression 3. Treatment of withdrawal
syndrome of morphine & heroin addicts.
D.
Diamorphine (heroin):
a semi synthetic drug made by acetylation of
morphine. It is the most powerful of all dependence producing drugs (very
imp.), because it's more lipophilic & enters the CNS readily & causes more
euphoria than morphine. t1/2 is 3 min. Metabolized into 2 active substances

19
Dr.Mohammed Qasim Mal-Allah
--> 6-acetyl-morphine & morphine. It is not given orally because of
complete pre-systemic or 1st pass metabolism, so by injection people
addicted on heroin are more liable to have viral hepatitis & AIDs. Its uses in
medicine are illegal.
E.
Fetanyl:
used in anesthesia.
II. Low to moderate efficacy group:
1.
Codeine:
tl/2 is 3 hrs. It is methyl morphine, naturally occurring low to
moderate efficacy opioids. In the body only 10% is converted to morphine,
so its action is 1/10 that of morphine (in same cone. of both).
It lacks efficacy to severe pain. It is used in cough suppression & for short term
systemic control of the acute diarrhea. It is usually combined with aspirin or
paracetamol & also with cough suppressants.
2. Dextropropoxyphene: t1/2 is 12 hrs. Analgesic effectiveness is equal to that
of codeine. The levo form has antitossive effect, but no analgesic effect. It is
less dependence-producing & less analgesic when compared to methadone.
It is rapidly absorbed & metabolized in liver. In over-dose it causes
respiratory depression & arrhythmia because of the quinidine-like action on
the heart. Combined with aspirin & paracetamol for greater analgesic effect.
Its effect is potentiated by alcohol.
C. Partial agonists (mixed):
1. Pentazocine: is a partial agonist at Kappa receptors & weak antagonists at µ
receptors & delta receptors. On sigma receptor produces dysphoria. It
produces withdrawal syndrome in morphine addicts. By itself it causes
psychological & physical dependence. Analgesic effect equals that of
morphine, but causes less euphoria. tl/2 is 3 hrs.
Adverse effects:
20
Dr.Mohammed Qasim Mal-Allah
Nausea, vomiting, sweating, dizziness, palpitation, tachycardia & hypertension &
dysphoria.
It is less liable to cause dependence than morphine.
Produces less respiratory depression.
Duration of action is shorter with less constipation.
Hypertension is both systemic & pulmonary, so we can't use it in treatment
of pulmonary edema --> acute pulmonary failure "imp.".
It's antagonized by naloxone.
2. Phenazocine: partial agonist, high efficacy opioid. The main use is in biliary
colic because; it causes less spasm of sphincter of Oddi.
3. Buprenorphine: high efficacy, partial agonist opioid acting on ~ receptors
with long duration of action of about 6-8hrs. t1/2 is 3hrs. Less liable to cause
dependence & respiratory depression & has little CVS effects.
Advantages: less spasm at the sphincter of Oddi, so causing no increase in
the intra-biliary pressure, also it's used in biliary colic treatment.
Disadvantages: although less likely to cause respiratory depression, but in
overdose this depression is "only partially antagonized" by the action of
naloxone.
4. Meptazinol: high efficacy partial agonist. It has central cholinergic activity
which probably adds to its analgesic effect. It relieves pain of moderate
intensity. Used post-operatively & in obstetrics. It causes no euphoria & no
withdrawal syndrome when it is discontinued. Even when given to patient
addicts on morphine, there will be no withdrawal syndrome.
5. Tramadol: tl/2 is 6hrs. It binds to µ receptors causing analgesia. It inhibits
neuronal nor-adrenaline uptake & serotonin release. It is effective orally &
as effective as pethidine for post-operative pain & less likely to cause
constipation & less addiction & respiratory depression. Only 20% of its conc

21
Dr.Mohammed Qasim Mal-Allah
undergoes 1
st
pass metabolism. It may cause convulsions, hallucinations &
probably anaphylaxis.
Opioid antagonists:
These include Naloxone, Naltrexone and Nalmefene.
1. Naloxone:
Pure competitive antagonist at u, Kappa & sigma receptors, but its potency
on Il receptors is 10 times_greater than on Kappa receptors .
It antagonizes both agonists & partial agonists
It is given I.V. only because of its high pre-systemic metabolism . ./ It
produces withdrawal syndrome in addicts on opioids .
When given I.V., it reverses opioid-induced respiratory depression within 1-
2 min & the duration of action is lhr .
Dose is 100-200 hrs .
Because opioid analgesic acts much longer than this (1hr), repeated I.V.
doses of naloxone of “100 mg” are required because the patient may recover
after a single dose of naloxone & appears normal only to relapse into coma
after 1-2 hrs. Response is shown by changes in respiratory rate, pupil
(disappearance of miosis & improvement of consciousness) (as the patient
may be comatous). Subsequent dose can be given I.M.
Other use: to counter excess the effect of opioids after surgical anesthesia &
after child birth (given to the baby).
Used in vascular endotoxic shock or (vascular septic shock).

22
Dr.Mohammed Qasim Mal-Allah
2. Naltrexone:
It is similar to naloxone but longer action (tl/2 is 4hrs)
Duration of action 2-3 days because the active metabolites have t1/2 of 13
hrs. .
Advantage on naloxone that it can be given orally.
It is also used to decrease craving for alcohol in chronic alcoholics.
3. Nalorphine:
Antagonist for all effects of morphine & other opioids.
It is partial antagonist(i.e.:- in normal subject it acts as weak agonist, but if
given to addict on morphine or other opioids which are stronger, then it acts
as antagonists to their effects.
4. Nalmefene: it is the newest of all these antagonists. It is a derivative of
naltrexone but given only I.V. It has a longer t1/2 than naloxone (8-10hrs.).
