1
THE THYROID
GLAND
د عمر فاروق العزاوي
2015 ‐ 2016

2
Physiology
The primary function of the thyroid is production of the hormones:
thyroxine (T
4
), Triiodothyronine (T
3
), and a small amount of reverse T3.
Upon stimulation by (TSH), the follicular cells synthesize thyroid hormones
by incorporating iodine into the amino acid tyrosine on the surface of
thyroglobulin (Tg).
A dietary intake of 125 μg/day is required to maintain thyroid function in
adults.
Calcitonin
Calcitonin is a hypocalcaemia peptide hormone. Calcitonin seems to be of
limited physiologic significance in humans, at least with regard to calcium
homeostasis. It is of medical significance because of its role as a tumor
marker in cases of medullary carcinoma and its medical use as an adjunctive
treatment in severe hypercalcemia and in Paget's disease of bone.
The hypocalcemic activity of calcitonin is by inhibition of osteoclast‐
mediated bone resorption and secondarily by stimulation of renal calcium
clearance. Calcitonin exerts additional effects in the brain, the
gastrointestinal tract, and the immune system, as an e.g analgesic effects in
the hypothalamus.
Synthesis of thyroid hormones
(1) Thyroglobulin (Tg) is synthesised and secreted into the colloid of the T4 is
converted to T3 by 5′‐monodeiodinase.
(2) Inorganic iodide (I
−
) is actively transported into the follicular cell
(trapping).
(3) Iodide is transported on to the colloidal surface by a transporter pendrin,
and ‘organified’ by the thyroid peroxidase enzyme, which incorporates it
into the amino acid tyrosine on the surface of Tg to form monoiodotyrosine
(MIT) and diiodotyrosine (DIT).
(4) Iodinated tyrosines couple to form T3 and T4.
(5) Tg is endocytosed and is cleaved by proteolysis to free the iodinated
tyrosine and thyroid hormones.
(6) Iodinated tyrosine is dehalogenated to recycle the iodide.
The thyroid secretes predominantly thyroxine (T4), with only a small
amount of triiodothyronine (T3) and rT3;
Approximately 85% of T3 in blood is produced from peripheral T4

3
conversion by monodeiodinase enzymes. So T4 can be regarded as a pro‐
hormone, since it has a
Longer half‐life in blood than T3 (approximately 1 week compared with
approximately 18 hours),
T4 binds and activates thyroid hormone receptors less effectively than
T3.
T4 can also be converted to the inactive metabolite, reverse T3 (rT3 is
not metabolically active, in fact it may interfering with T3 & T4
function).
T3 is four mes more potent than T4.
So T4 acts as a steady, supply that can be converted to the more potent
hormone as needed.
More than 99% of T3 and T4 circulate in plasma, bound to transport
proteins, mainly thyroxine‐binding globulin (TBG), and to a lesser extent
transthyretin, and albumin.
It is the unbound or free hormones which diffuse into tissues and exert the
metabolic actions as
Increased metabolic rate
Adrenergic action, e.g. on heart rate, gut motility CNS activation
Bone demineralization, Osteoporosis.
Cellular differentiation etc.
Presenting problems in thyroid disease
Thyroid disorders may present with or without enlargement of the
thyroid gland (goitre), the goitre may be
Nodular (single or multiple) or difuse.
And they may be euthyroid, hypothyroid or hyperthyroid.
Diagnosis of thyroid disease
I) The medical history and physical exam are important parts of the
evaluation for thyroid problems, focusing on the eyes, skin, heart, and
neurologic findings etc.
II) Blood tests
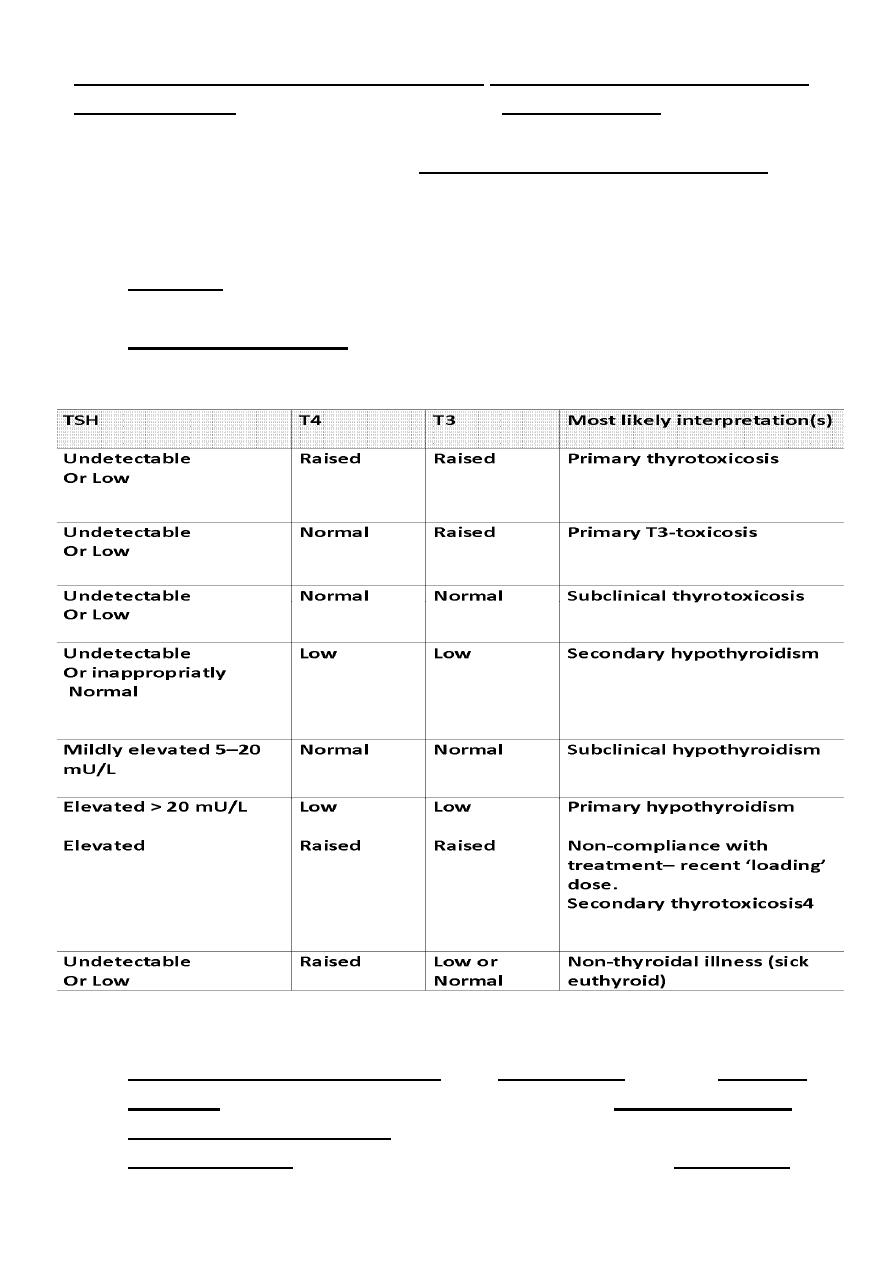
Thyroid‐stimulating hormone (TSH): TSH is usually regarded as the
most useful investigation of thyroid function.
When there is an excess of thyroid hormone in the blood, as in
hyperthyroidism, the TSH is suppressed or undetected (negative
feedback). And the opposite is true.
4
TSH may take several weeks to ‘catch up’ with changes in T4 and T3 levels
after treatment, so for follow up you need T4 and T3 levels.
Circadian rhythm of TSH secretion is present but the variation is small so it
can be assessed from a single blood sample taken at any time and does not
require any stimulation or suppression.
Free (T4): High T4 may indicate hyperthyroidism. Low T4 may indicate
hypothyroidism.
Triiodothyronine (T3): High T3 may indicate hyperthyroidism. Low T3
may indicate hypothyroidism.
TSH receptor antibodies (TRAb) is an IgG antibody that can cross the
placental barrier. TRAb autoantibodies are most closely associated
with disease pathogenesis. TSH receptor antibodies (TRAb) can be
stimulatory (TSI), causing Graves’ thyrotoxicosis, or an antagonists
(TRAb ‐blocking antibodies), causing hypothyroidism.

5
Thyroid‐stimulating immunoglobulins (TSI), are also known as long‐
acting‐thyroid‐stimulator independent of the normal feedback,
it is present in Grave's disease mainly (+ve in 80–95%), the sensi vity
and specificity are >90%,
It may also be +ve in 10–20% of pa ents with Autoimmune
hypothyroidism especially TRAb ‐blocking antibodies.
Thyroid peroxidase Antibody (TPO): This antibody is present in patients
with Autoimmune hypothyroidism (+ve in 90–100 %), and may also be
+ve in 50–80% of pa ents with Grave's disease.
Also may be +ve in normal population, multinodular goitre, transient
thyroiditis so less sensitive and less specific.
Thyroglobulin Antibody(Tg): +ve in normal population, grave's disease,
multinodular goitre, transient thyroiditis, so less sensitive and less
specific.
The role of both TPO and Tg in the disease pathogenesis is less well
established.
III) Thyroid ultrasound: Thyroid ultrasound helps to determine the size,
surface, number as well as the different types of nodules in the thyroid
gland.
It can discriminate the diffuse goitre of Graves’ disease from the irregular
enlargement of a multinodular goitre or a solitary nodule .
This exam can also detect if there are enlarged parathyroid glands or lymph
nodes.
IV) Nuclear thyroid scan: During this scan radioactive
123
I or
99m
technetium,
is used and then an imaging study of the thyroid is done.
Increased uptake with thyrotoxic function test, indicates
hyperthyroidism,
While low uptake and a hypothyroid function test indicates
hypothyroidism.
Low‐uptake with a thyrotoxic function test, indicates thyrotoxic phase
of transient thyroiditis.
This test should not be performed on women who are pregnant.
99m
technetium scans, are quicker to perform with a lower dose of
radioactivity, and provide a higher‐resolution image.

6
gauge needle, usually making several passes
‐
21
needle aspiration:
‐
V) Fine
through different parts of the nodule, and sent for histopathological study.
used to look
occasionally
is
(CT) scan:
Computerized axial tomography
VI)
for the extent of a goiter into the upper chest or to look for narrowing or
displacement of the trachea.
Thyrotoxicosis
Is a condition caused by an excess of thyroid hormones from any cause.
Hyperthyroidism
is a condition in which an overactive thyroid gland is
producing excessive amount of thyroid hormones.
Causes pf Thyrotoxicosis
The most common causes are Graves’ disease, toxic multinodular goitre and
autonomously
functioning
Solitary thyroid
adenoma (nodule)
respectivly.
Other causes are

7
Graves' Disease
Is the most common cause of hyperthyroidism 78%. In this condi on, the
thyroid gland has lost the ability to respond to the normal control by the
TSH.
Graves' disease 5 mes more common among women than men.
Grave‘s disease is considered an autoimmune disease, and antibodies are
found in the blood.
These antibodies include thyroid stimulating immunoglobulin (TSI
antibodies), thyroid peroxidase antibodies (TPO), and TRAb ‐blocking
antibodies.
The triggers for Grave's disease include: stress/smoking/radiation to the
neck, medications, and infectious organisms such as viruses.
Grave's disease may be associated with eye disease (Graves'
ophthalmopathy), and other characteristic signs mentioned later.
Ophthalmopathy can occur before, after, or at the same time as the
hyperthyroidism. Early symptoms are sensitivity to light and a feeling of
"sand in the eyes."
The eyes may protrude and double vision can occur (diplopia). The degree of
ophthalmopathy is worsened in those who smoke or treated by radiation.
The course of the eye disease is often independent of the thyroid disease,
and steroid therapy may be necessary to control the inflammation. In
addition, surgical intervention may be required.
Functioning Adenoma
A single nodule becomes "autonomous" and does not respond to pituitary
regulation via TSH and produces thyroid hormones independently.
The toxic solitary nodule is the cause of less than 5% of all cases of
thyrotoxicosis. The nodule is a follicular cell adenoma, which autonomously
secretes excess thyroid hormones and inhibits endogenous TSH secretion
with subsequent atrophy of the rest of the thyroid gland.
The adenoma is usually greater than 2‐3 cm in diameter.
Most patients are females and over 40 years of age.
Although many nodules are palpable, the diagnosis can be made with
certainty only by isotope scanning.
131
I is highly effective and is an ideal treatment since the atrophic cells
surrounding the nodule do not take up iodine and so receive little or no
radiation. For this reason, permanent hypothyroidism is unusual. A surgical
hemithyroidectomy is an alternative.

8
Toxic Multinodular Goiter
multinodular goiter becomes "autonomous" and does not respond to
pituitary regulation via TSH and produces thyroid hormones independently
(More explaIned later).
Excessive intake of thyroid hormones
Taking too much thyroid hormone medication is actually quite common.
Excessive doses of thyroid hormones frequently go undetected due to the
lack of follow‐up of patients taking their thyroid medicine.
Other persons may be abusing the drug in an attempt to achieve other
goals.
Abnormal secretion of TSH
A tumor in the pituitary gland may produce an abnormally high secretion of
TSH, this leads to excessive signaling to the thyroid gland to produce thyroid
hormones. This condition is very rare and can be associated with other
abnormalities of the pituitary gland.
Excessive iodine intake
An excess of iodine may cause Iodine‐induced hyperthyroidism or
hypothyroidism, and is usually seen in patients who already have an
underlying abnormal thyroid gland. Certain medications, such as
amiodarone, which is used in the treatment of heart problems, contain a
large amount of iodine and may be associated with thyroid function
abnormalities.
Clinical manifestations of all Thyrotoxicosis
The most common symptoms are
weight loss with a normal or
increased appetite, heat intolerance,
sweating, palpitations, tremor and
irritability.
In patients older than 70 years, the
typical signs and symptoms may be
absent and only present with
irregular heart rhythms and heart
failure Other symptoms are

9
Signs
Common signs for all causes of thyrotoxicosis are Weight loss, Tremor
Palmar Erythema, Sinus
tachycardia, lid retraction, lid
lag.
All causes of thyrotoxicosis can
cause lid retraction and lid lag,
due to potentiation of
sympathetic innervations of the
levator palpebrae muscles.
Other signs are
Signs characteristic of Graves’ disease:
Ophthalmopathy, including
periorbital edema, conjunctival irritation, exophthalmos and diplopia.
Thyroid Acropachy (rare periosteal hypertrophy, indistinguishable from
finger clubbing)
Thyroid Dermopathy (Pretibial Myxedema) This skin condition is rare
and is due to deposition of glycosaminoglycans in the dermis of the lower
legs causing nonpitting edema, which is usually associated with
erythema and thickening of the skin, without pain or pruritus that
appears on the shins of the legs and tops of the feet.
Thyroid Bruit.
Diagnosis of Thyrotoxicosis
Clinical manifestations and signs
Investigations
The first‐line investigations are serum T3, T4 and TSH.
The main tool for detection of hyperthyroidism is measurement of the TSH
level. Which is low or undetectable except in secondary hyperthyroidism.
Measurement of TSH receptor antibodies (TRAb, elevated in Graves’
disease).
Others if needed as U. S and isotope scanning,
Other none specific Investigations as
ECG may demonstrate sinus tachycardia or atrial fibrillation.
High bl.sugar, …… etc .

10
Treatment
The options for treating hyperthyroidism include:
1. Trea ng the symptoms
2. An thyroid drugs
3. Radioac ve iodine
4. Surgery
1.Trea ng the symptoms
By beta‐blockers to decrease rapid heart rate and if used in high doses (only
Propranalol), it decrease peripheral T4 to T3 conversion.
2. An thyroid Drugs
There are two main antithyroid drugs available for use, methimazole and
propylthiouracil (PTU). These drugs block production of thyroid hormones in
the thyroid. PTU also blocks peripheral conversion of T4 to T3.
The major risk of these medications is occasional suppression of white blood
cells production by the bone marrow (agranulocytosis).
It is important for patients to know that if they develop a fever, a sore
throat, or any signs of infection while taking methimazole or
propylthiouracil, they should see a doctor immediately.
The actual risk of developing agranulocytosis is less than 1%
long‐term Antithyroid therapy is only used for Graves' disease, since this
disease may actually go into remission in 40%‐70% a er 1‐2y of treatment.
Relapse of Graves' dis a er stopping treatment is most likely in the 1
st
year.
If a patient does relapse, antithyroid drug therapy can be restarted for a
longer period, or radioactive iodine or surgery may be considered.
3. Radioac ve Iodine
131
I is used to ablate a hyperactive gland.
It is the treatment of choice for
Recurring Graves' disease,
Patients with severe cardiac involvement,
Multinodular goiter or toxic adenomas,
Patients who cannot tolerate antithyroid drugs.
It takes 8 to 12 weeks for the thyroid to become normal after therapy.
Since iodine is only picked up by thyroid cells, the destruction is local, and
there are no widespread side effects with this therapy.
Not used in pregnancy and breast‐feeding. and used with caution in patients
with Graves' eye disease since eye disease may worsen after therapy.

11
Permanent hypothyroidism is the major complication of this form of
treatment. While a temporary hypothyroid state may be seen up to six
months after treatment,
4. Surgery is appropriate for:
Pregnant patients
Children who have major adverse reactions to Antithyroid drugs.
Patients with very large thyroid glands and in those who have
symptoms from compression of tissues adjacent to the thyroid, such as
difficulty swallowing, hoarseness, and shortness of breath.
The major complication of surgery is disruption of the surrounding
tissue, including the
Nerves supplying the vocal cords
Parathyroid glands
Thyroid Crises (Thyroid storm)
Thyroid storm is an acute form of hyperthyroidism that results from either
unrecognized untreated or inadequately treated severe hyperthyroidism. It
is a rare medical emergency, which has a mortality of 10% despite early
recognition and treatment.
Precipitated by infection, trauma, surgery, or any other stressful condition
Present with florid symptoms of hyperthyroidism with one or more of the
following: fever, agitation confusion, psychosis, coma, tachycardia or atrial
fibrillation, cardiovascular collapse and shock.
Treatment of Thyroid Storm
Patients should be rehydrated
Give propranolol, either orally (80 mg 4 mes daily) or intravenously
(1–5 mg 4 mes daily). It helps in controlling adrenergic symptoms and
also reduces the peripheral conversion of T4 to T3 (propranolol only in
high doses).
Sodium ipodate (500 mg per day orally) will restore serum T3 levels to
normal in 48–72 hours (inhibits the release of thyroid hormones, and
reduces the peripheral conversion of T4 to T3).
Dexamethasone (2 mg 4 mes daily) also reduces the peripheral
conversion of T4 to T3.
Oral carbimazole 40–60 mg daily should be given to inhibit the
synthesis of new thyroid hormone.

12
If the patient is unconscious or uncooperative, carbimazole can be
administered rectally with good effect.
Atrial fibrillation in thyrotoxicosis
Occurs in about 10% of patients with thyrotoxicosis. The incidence increases
with age, so that almost half of all males with thyrotoxicosis over the age of
60 are affected.
Characteristically and specifically, the ventricular rate is little influenced by
digoxin, but responds to the addition of a β‐blocker.
Thromboembolic complications are also common in thyrotoxic atrial
fibrillation so anticoagulation is required.
Subclinical thyrotoxicosis
Serum TSH is undetectable or very low, and serum T3 and T4 are at the
upper end of the normal range.
This is most often found in older patients with multinodular goitre.
These patients are at increased risk of atrial fibrillation and osteoporosis,
and hence the consensus view is that they have mild thyrotoxicosis and
require therapy, usually with
131
I.
Otherwise, annual review is essential, as the conversion rate to overt
thyrotoxicosis is about 5% each year.
Hypothyroidism
Hypothyroidism is a state of thyroid hormone deficiency.
Occurs at any age but is particularly common among the elderly,
10% of women and 6% of men > 65 are affected.
In all age group women are 6 mes more frequently affected than men.
It is either Primary or secondary.
Causes:
The most common cause of
Primary hypothyroidism is
Autoimmune disease that usually results from Hashimoto's thyroiditis.
The 2nd most common cause is post‐therapeutic hypothyroidism,
Following
131
I ,
Surgical treatment of thyrotoxicosis and goiter
Overtreatment with antithyroid drugs.
Both above accounts for over 90% of causes,

13
others are
Secondary hypothyroidism
occurs when the hypothalamus
produces insufficient thyrotropin‐
releasing hormone (TRH) or the
pituitary produces insufficient
TSH.
Clinical features of hypothyroidism
Symptoms and signs of primary hypothyroidism are often subtle and
insidious.
It may manifest atypically in the elderly as confusion, anorexia, weight loss,
incontinence, and decreased mobility.
The clinical presentation depends on the duration and severity of the
disease.
A prolonged duration of Hypothyroidism, leads to the infiltration of many
body tissues by
Mucopolysaccharides,
Hyaluronic acid
And chondroitin sulphate,
Resulting in a low‐pitched voice, slurred speech due to a large tongue, poor
hearing, and compression of the median nerve at the wrist (carpal tunnel
synd with paresthesias of the hands).
Infiltration of the dermis gives rise to non pitting edema (myxedema), which
is most marked in the skin of the hands, feet, face and eyelids . Resulting in
periorbital and facial puffiness with dull facial expression combined with
facial pallor due to
Vasoconstriction or
Anemia (B12 or iron deficiency),
Or a lemon‐yellow tint of the skin caused by carotenaemia.

14
Other symptoms are
Clinical signs are
Investigations
In Primary hypothyroidism, the serum T4 is low and TSH is elevated,
usually in excess of 20 mU/L.
Measurements of serum T3 are unhelpful since they do not
discriminate reliably between euthyroidism and hypothyroidism.
Measurement of thyroid peroxidase antibodies although +ve in many
different etiologies is some times helpful.
Other non‐specific abnormalities are
Raised serum enzymes: creatine kinase, aspartate aminotransferase,
lactate dehydrogenase (LDH)

15
Hypercholesterolemia
Anemia: normochromic normocytic or macrocytic
Hyponatremia
ECG classically demonstrates sinus bradycardia with low‐voltage
complexes and ST segment and T‐wave changes.
Treatment
Is with Levothyroxine (T4) replacement.
In patients with known ischemic heart disease and elderly, thyroid
hormone replacement should be introduced at low dose 25 μg per day,
and increased very slowly, to finally reach maintenance dose of 100–
150 μg per day.
In younger patients, it is safe to initiate levothyroxine at a higher dose
100 μg per day.
Aim to maintain serum TSH within the reference range, and to achieve
this, serum T4 should be in the upper normal range.
Levothyroxine (T4) has a half‐life of 7 days so it should always be taken
as a single daily dose, absorption is maximal when the dose is taken
before bed and may be further optimized by taking vitamin C.
At least 6 weeks should pass before repeating thyroid function tests
and adjus ng the dose, usually by 25 μg/day.
Measure thyroid function every 1–2 years once the dose of T4 is
stabilized.
Patients feel be er within 2–3 weeks. Reduction in weight and
periorbital puffiness occurs quickly, but the restoration of skin and hair
texture and resolu on of any effusions may take 3–6 months.
Situations in which an adjustment of the dose of T4 is necessary are
1‐ Pregnancy
• Increases concentration of serum thyroxine‐binding globulin, require
an increase in the dose of levothyroxine of approximately 25–50 μg,
Inadequate maternal T4 therapy may be associated with impaired
cognitive development in an unborn child.
2‐ Malabsorption
3‐ Drugs
• Drugs that Increase T4 clearance: Phenobarbital, phenytoin,
carbamazepine, rifampicin, sertraline, chloroquine.
• Drugs Interfere with intestinal T4 absorp on: colestyramine,
calcium carbonate …..etc.

16
SUBCLINICAL HYPOTHYROIDISM
Is elevated serum TSH in patients with absent or minimal symptoms of
hypothyroidism and normal serum levels of free T4.
It is relatively common; occurs in more than 15% of elderly women and 10%
of elderly men.
In patients with serum TSH > 10 mU/L, there is a high likelihood of
progression to overt hypothyroidism.
These patients are also more likely to have hypercholesterolemia and
atherosclerosis. They should be treated with T4, even if they are
asymptomatic.
For patients with TSH levels between 4.5 and 10 mU/L, use of T4 is
reasonable if symptoms of early hypothyroidism (eg, fatigue, depression)
are present, therapy is also indicated in pregnant and women who plan to
become pregnant to avoid effects of hypothyroidism on the pregnancy and
fetal development. Patients should have annual measurement of serum TSH
and free T4 to assess progress of the condi on if untreated or to adjust the
T4 dosage.
Non‐thyroidal illness (‘sick euthyroidism’)
This presents with a low serum TSH, raised T4 and normal or low T3, in a
patient with systemic illness who doesn't have clinical evidence of thyroid
disease.
These abnormalities are due to
Decreased peripheral conversion of T4 to T3,
Altered levels of binding proteins and their affinity for thyroid
hormones,
Reduced secretion of TSH.
Myxedema coma
The condition usually occurs in patients with long‐standing, undiagnosed
hypothyroidism and is usually precipitated by infection, cerebrovascular
disease, heart failure, trauma, or drug therapy.
It has a 50% mortality rate and needs urgent treatment.
Pathophysiology
long‐standing hypothyroidism is associated with reduced metabolic rate and
decreased oxygen consumption, which affects all body systems resulting in
Hypothermia,
Cardiac contractility is impaired, leading to reduced stroke volume, low
cardiac output, bradycardia, hypotension and pericardial effusions.

17
Respiratory depression (Central), Hypoventilation with CO2 reten on.
Brain function is affected by
Reduction in oxygen delivery
Decreased glucose utilization
Reduced cerebral blood flow.
Rapid diagnosis based on clinical judgment, history, and physical
examination is imperative, because death is likely without rapid treatment.
So treatment must begin before biochemical confirmation of the diagnosis.
Treatment
Maintenance of adequate airway is crucial, since most patients have
depressed mental status with respiratory failure. Mechanical
ventilation is usually required during the first 36‐48 hours,
Intravenous injection of 20 μg triiodothyronine(T3) three times daily
until there is sustained clinical improvement.
Or an intravenous loading dose of 300‐600 micrograms of
levothyroxine (T4) followed by a daily intravenous dose of 50‐100
micrograms.
Corticosteroids are also given, because the possibility of central (2ndry)
hypothyroidism usually cannot be initially ruled out.
Treat hypothermia with passive rewarming using ordinary blankets
and a warm room. Active rewarming using external devices carries a
risk of vasodilatation and worsening hypotension and should be
avoided.
The precipitating factor should be rapidly treated.
Thyroid lump or Thyroid swelling or Goiter
A common thyroid problem, affecting about 5% of the population that
present as a lump in the neck or sometimes present with acute painful
enlargement of the thyroid.
There are 3 main types
1‐ Diffuse goiter
2‐ Multinodular goitre
3‐ Solitary nodule.
1‐ Diffuse goitre
A‐ Simple goitre
This form of goitre usually presents between the ages of
15 and 25 years.
It occurs sporadically and is of unknown aetiology.

18
The goitre is soft and symmetrical and the thyroid is enlarged to 2‐3 times its
normal size.
There is no tenderness, no lymphadenopathy, no bruit.
T3,T4 and TSH are normal and no thyroid autoantibodies.
A diffuse goitre rarely needs further treatment, and in most cases the
goitre regresses, unless it is very large and causing cosmetic symptoms or
compression of other local structures (resulting in stridor or dysphagia).
Thyroxine therapy is sometimes justified in an attempt to shrink the goitre.
In some, however, the unknown stimulus to thyroid enlargement persists
and, as a result of recurrent episodes of hyperplasia and involution during
the following 10–20 years, the gland becomes multinodular with areas of
autonomous function (Multinodular goitre).
B‐ Hashimoto’s thyroiditis
Thyroiditis refers to an inflammation of the thyroid.
It is characterised by Permanent destructive lymphoid infiltration of the
thyroid, leading to a varying degree of fibrosis and thyroid enlargement.
Hashimoto’s thyroiditis increases in incidence with age and affects
approximately 3.5 per 1000 women and 0.8 per 1000 men each year. Many
present with a small or moderately sized diffuse goitre, which is
characteristically firm or rubbery in consistency. It is sometimes impossible
to differentiate it from simple goitre by palpation alone. Around 25% of
patients are hypothyroid at presentation. In the remainder, serum T4 is
normal and TSH normal, but these patients are at risk of developing overt
hypothyroidism in future years.
Anti‐thyroid peroxidase antibodies are present in the serum in more than
90% of patients with Hashimoto’s thyroiditis.
In those under the age of 20 years, antinuclear factor (ANF) may also
be positive.
Thyroxine therapy is indicated as treatment for hypothyroidism, and also to
shrink an associated goitre.
Although rare there is an increased risk of thyroid lymphoma.
Spontaneous atrophic hypothyroidism
A term used for hypothyroid patients without a goitre in whom TSH
receptor‐blocking antibodies may be more important than anti‐
peroxidase antibodies.

19
However, these 2 above conditions can both be considered as variants of
the same underlying disease process, and sometimes are given the
nomenclature of autoimmune hypothyroidism.
C‐ Transient thyroiditis
is of many types
i‐ Subacute (de Quervain’s) thyroiditis
In its classical painful form, subacute thyroiditis is a transient
inflammation of the thyroid gland occurring after infection with Coxsackie,
mumps or adenoviruses.
There is pain in the region of the thyroid that radiate to the angle of the jaw
and the ears, and is made worse by swallowing,
coughing and movement of the neck. The thyroid is usually palpably
enlarged and tender. Systemic
upset (fever…..etc) is common. Affected patients are usually females
aged 20–40 years.
ii‐ Silent thyroiditis
Is an other form of transient thyroiditis, it is Painless. Can also occur after
viral infection and in patients with underlying
autoimmune disease
iii‐ Drug‐induced thyroiditis
Transient thyroiditis that can be precipitated by drugs, including interferon‐
α and lithium. Symptoms continue as long as the drug is taken.
iv‐ Acute thyroiditis
(also called suppurative thyroiditis)
Transient thyroiditis caused by bacteria or other infectious organisms.
Symptoms include a painful thyroid, generalized illness and occasionally
symptoms of mild hypothyroidism.Symptoms improve after treatment of
the infectious cause.
v‐ Post‐partum thyroiditis
The maternal immune response, which is modified during pregnancy to
allow survival of the fetus, is enhanced after delivery and may unmask
previously unrecognized auto antibodies that attack the thyroid after
delivery of a child.
Symptoms of thyroid dysfunction are rare . However, symptomatic
thyrotoxicosis presenting for the first me within 12 months of childbirth is

20
likely to be due to post‐partum thyroiditis and the diagnosis is confirmed by
a negligible radioisotope uptake. The clinical course and treatment are
similar to painless subacute thyroiditis. Post‐partum thyroiditis tends to
recur after subsequent pregnancies and eventually patients progress over a
period of years to permanent hypothyroidism.
In most types of Transient thyroiditis above, inflammation in the thyroid
gland occurs and is associated with release of colloid and stored thyroid
hormones, with damage to follicular cells and impaired synthesis of new
thyroid hormones. As a result, T4 and T3 levels are raised for 4–6 weeks
until the preformed colloid is depleted. Thereafter, there is usually a period
of hypothyroidism of variable severity until follicular cells recover and
normal thyroid function is restored within 4–6 months.
During this time there is no radioisotope uptake, because the damaged
follicular cells are unable to trap iodine and because TSH secretion is
suppressed.
Low‐titer thyroid autoantibodies appear transiently in the serum, and the
erythrocyte sedimentation rate (ESR) is usually raised.
The pain usually respond to simple non‐steroidal anti‐inflammatory drugs
(NSAIDs). Occasionally, it may be necessary to prescribe prednisolone 40 mg
daily for 3–4 weeks.
The thyrotoxicosis is mild and treatment with a β‐blocker is usually
adequate. Antithyroid drugs are of no benefit because thyroid hormone
synthesis is impaired rather than enhanced. Careful monitoring of thyroid
function and symptoms is required so that thyroxine can be prescribed
temporarily in the hypothyroid phase.
D‐ Iodine‐associated thyroid disease
i‐ Iodine deficiency
Thyroid enlargement is extremely common in certain mountainous parts of
the world, where there is dietary iodine deficiency (endemic goitre). Most
patients are euthyroid with normal or raised TSH levels, although
hypothyroidism can occur with severe iodine deficiency.
Iodine supplementation programmes have abolished this condition in most
developed countries.

21
ii‐ Iodine‐excess thyroid dysfunction
Excess iodide (Dietary or as a diagnostic contrast medium for the thyroid or
any other organs) transiently inhibits thyroid iodide organification, in
individuals with a normal thyroid, this phenomenon is known as the Wolff‐
Chaikoff effect, which lasts 2–3 wks, after which it is followed by an 'escape
phenomenon', leading to the resumption of normal organification of iodine
and normal thyroid function, so the normal gland escapes from this
inhibitory effect and iodide organification resumes.
But in patients with abnormal gland one of the following may occur:
1‐ Iodine‐Induced Hypothyroidism due to failure of the thyroid to escape
from the Wolff–Chaikoff effect, in individuals with pre‐existing thyroid
disease not clinically apparent.
The susceptible individuals are as follows:
Previously treated Euthyroid Graves' disease,
Hashimoto's thyroiditis,
History of subacute, or postpartum thyroiditis, etc.
2‐ Iodine‐Induced Hyperthyroidism
In which patients with pre‐existing thyroid problem, becomes hyperthyroid
after exposure to iodine and this is called the (Jod‐Basedow phenomenon),
The Jod‐Basedow phenomenon is hyperthyroidism following administration
of iodine , either as a dietary supplement or as a contrast medium.
This phenomenon typically present in some patients with
Endemic goiter (due to iodine deficiency), who relocate to an iodine‐
abundant geographical area.
Graves disease,
Toxic multinodular goiter,
Thyroid adenoma
Administration of amiodarone.
The Jod‐Basedow effect does not occur in persons with normal thyroid
glands
The Jod‐Basedow phenomenon is the opposite of the Wolff‐Chaikoff effect.
Amiodarone
The anti‐arrhythmic agent amiodarone affect the thyroid by
Has a structure that is analogous to T4.
Contains huge amounts of iodine; a 200 mg dose contains 75 mg
iodine, compared with a daily dietary requirement of just 125 μg.
Amiodarone also has a cytotoxic effect on thyroid follicular cells.

22
Inhibits conversion of T4 to T3.
Only 20% of patients receiving amiodarone develop hypothyroidism or
thyrotoxicosis and so thyroid function should be monitored regularly.
The thyrotoxicosis can be classified as either:
• type I: a Jod–Basedow effect in patients with underlying thyroid disease,
or
• type II: thyroiditis due to cytotoxicity, resulting in a transient
thyrotoxicosis.
These patterns can overlap and can be difficult to distinguish clinically, as
iodine uptake is low in both. There is no widely accepted management
algorithm,
Antithyroid drugs may be effective in patients with the type I form, but are
ineffective in type II thyrotoxicosis. Prednisolone is beneficial in the typeII
form.
A pragmatic approach is to commence combination therapy with an
antithyroid drug and glucocorticoid in patients with significant
thyrotoxicosis. A rapid response (within 1–2 weeks) usually indicates a type
II picture and permits withdrawal of the antithyroid therapy;
a slower response suggests a type I picture, when antithyroid drugs may be
continued and prednisolone withdrawn.
Aamiodarone should be discontinued.
2‐ Multinodular goitre
Patients with thyroid enlargement in the absence of thyroid dysfunction or
positive autoantibodies (i.e. ‘simple goitre’) may progress to develop
nodules. These nodules grow at varying rates and secrete thyroid hormone
‘autonomously’, thereby suppressing TSH‐dependent growth and function in
the rest of the gland. Ultimately, complete suppression of TSH occurs in
about 25% of cases, with T4 and T3 levels o en within the normal range
(subclinical thyrotoxicosis) but sometimes elevated (toxic multinodular
goitre). Opinions differ as to whether the nodules represent multiple
adenomas or focal hyperplasia.
There are reports that the prevalence of foci of thyroid cancer is increased in
multinodular goitres, but for practical purposes patients can be reassured
that it is a benign condition and malignancy need only be considered in
patients with a large ‘dominant’ nodule that is ‘cold’ (i.e. does not take up
radioisotope).

23
Clinical features and investigations
Multinodular goitre is usually diagnosed in patients presenting with
thyrotoxicosis, a large goitre or sudden painful swelling caused by
haemorrhage into a nodule or cyst.
Very large goitres may cause mediastinal compression with stridor,
dysphagia and obstruction of the superior vena cava.
Hoarseness due to recurrent laryngeal nerve palsy can occur, but is far more
suggestive of thyroid carcinoma.
The diagnosis can be confirmed by a radioisotope thyroid scan and/or
ultrasonography.
In those with a ‘dominant’, ‘cold’ nodule, fine needle aspiration is indicated
to exclude thyroid cancer.
Management
If the goitre is small and non toxic, no treatment is necessary, but only
annual follow up.
Partial thyroidectomy is indicated for large Goitres, or
131
I for old
people.
Thyroxine therapy is of no benefit in shrinking multinodular goitres
and may simply aggravate any associated thyrotoxicosis.
In toxic multinodular goitre treatment is usually with
131
I or surgery.
3‐ Solitary thyroid nodule
It is important to determine whether the nodule is benign or malignant. It is
rarely possible to make this distinction on clinical grounds alone, the
presence of the following increase the suspicion,
Cervical lymphadenopathy
Presenting in childhood or adolescence,
Past history of head and neck irradiation,
Presenting in the elderly.
Investigations
Serum T3, T4 and TSH should be measured in all patients
with a solitary thyroid nodule.
The finding of undetectable TSH is very suggestive of a benign autonomously
functioning thyroid follicular adenoma (Toxic adenoma), but this diagnosis
can only be confirmed by thyroid isotope scanning which will show hot
nodule in Toxic adenoma and Cold nodule in euthyroid or hypothyroid
patients.
Yhe most useful investigation is fine needle aspiration of the nodule.

24
Cytological examination
can differentiate benign (80%) from definitely
malignant or indeterminate nodules (20%).
Of these 20%, about 25–50% are confirmed as cancer at surgery.
Management
Solitary nodules in which cytology either is inconclusive or shows malignant
cells are treated by surgical excision.
Benign euthyroid lesions are sometimes excised, if they are growing, but the
majority of patients can be reassured without treatmet. Benign toxic
nodules is mentioned before.
Thyroid malignancy
Primary thyroid malignancy is rare, accounting for less than 1% of all
carcinomas, It can be classified according to the cell type of origin.
With the exception of medullary carcinoma, thyroid cancer is more
common in females.
Papillary carcinoma
This is the most common of the malignant thyroid tumours, usually are
irradiation‐induced thyroid cancer. It may be multifocal and spread is to
regional lymph nodes. Some patients present with cervical
lymphadenopathy and no apparent thyroid enlargement.
Follicular carcinoma
This is always a single encapsulated lesion. rare metastases to lymph nodes
because metastases are blood‐borne and are most often found in bone,
lungs and brain.
Management of above 2
This is usually by total thyroidectomy followed by
large dose of
131
I to ablate any remaining thyroid tissue, normal or
malignant.
Thereafter, long‐term treatment with thyroxine in a dose sufficient to
suppress TSH (usually 150–200 μg daily) this is important, as there is
evidence that growth of differentiated thyroid carcinomas is TSH
dependent.
Follow up is by measurement of serum thyroglobulin, which should be
undetectable in patients whose thyroid has been ablated and who are
taking a suppressive dose of thyroxine. Detectable thyroglobulin is
suggestive of tumour recurrence or metastases, which may be localised

25
by whole‐body scanning with
131
I and may respond to further radio‐
iodine therapy.
Prognosis
Most patients have an excellent prognosis when treated appropriately.
Those under 50 years of age with papillary carcinoma have a near‐normal
life expectancy if the tumour is less than 2 cm in diameter, confined to the
thyroid and cervical nodes, and of low‐grade malignancy histologically. Even
for patients with distant metastases at presenta on, the 10‐year survival is
approximately 40%.
Medullary carcinoma
This tumour arises from the parafollicular C cells of the thyroid. In addition
to calcitonin, the tumour may secrete 5‐hydroxytryptamine (5‐HT,
serotonin), tachykinin peptides, ACTH and prostaglandins.
As a consequence, carcinoid syndrome and Cushing’s syndrome may occur.
Patients usually present in middle age with a firm thyroid mass. Cervical
lymphadenopathy is common, but distant metastases are rare initially.
Serum calcitonin levels are raised and are useful in monitoring response to
treatment. Despite the very high levels of calcitonin foundin some patients,
hypocalcaemia is extremely rare.
Treatment is by total thyroidectomy with removal of affected cervical
nodes. Since the C cells do not concentrate iodine, there is no role for
131
I
therapy.
Prognosis is very variable, some pa ents surviving 20 years or more and
others less than 1 year. Medullary carcinoma of the thyroid may occur
sporadically, or in families as part of the MEN type 2 syndrome.
Riedel’s thyroiditis
This is not a form of thyroid cancer, but the presentation is similar and the
differentiation can usually only be made by thyroid biopsy. It is an
exceptionally rare condition of unknown aetiology in which there is
extensive infiltration of the thyroid and surroundingstructures with fibrous
tissue. There may be associated mediastinal and retroperitoneal fibrosis.
Presentation is with a slow‐growing goitre which is irregular and stony‐
hard. There is usually tracheal and oesophageal compression necessitating
partial thyroidectomy.
Other recognised complications include recurrent laryngeal nerve palsy,
hypoparathyroidism and eventually hypothyroidism.
